题目内容
20.下列实验装置和操作能达到实验目的是( )| A. | 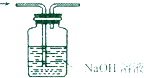 除去CO2中的HCl气体 | B. | 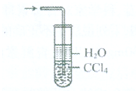 吸收NH3 | ||
| C. |  灼烧海带灰 | D. |  乙醇和水的分离 |
分析 A.CO2、HCl均与氢氧化钠溶液反应;
B.氨气不溶于四氯化碳;
C.灼烧用坩埚;
D.乙醇和水能形成共沸物.
解答 解:A.CO2、HCl均与氢氧化钠溶液反应,不能达到除杂的目的,应选用饱和碳酸氢钠,故A错误;
B.氨气不溶于四氯化碳,可防止倒吸,故B正确;
C.灼烧用坩埚,不用烧杯,故C错误;
D.乙醇和水能形成共沸物,应加氧化钙后再蒸馏,故D错误.
故选B.
点评 本题考查化学实验方案的评价,涉及除杂、混合物的分离等知识点,注重基础知识的考查,题目难度不大,选项B为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列各组微粒中,互为同素异形体的是( )
| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{13}$C | B. | H2O和D2O | ||
| C. | O2与O3 | D. | CH3OCH3与CH3CH2OH |
15.下列说法不正确的是( )
| A. | 面粉增白剂中的成份CaO2具有强氧化性 | |
| B. | CaO能与SO2反应,可用作工业废气的脱硫剂 | |
| C. | 新能源汽车的推广与使用有助于减少光化学烟雾的产生 | |
| D. | PM2.5是指空气中直径≥2.5μm的颗粒物,它们分散在空气中形成胶体 |
5.X、Y、Z、W四种元素在元素周期表中的相对位置如下图所示,其中X、W的质子数之和为21,由此可知( )
| X | Y | ||
| Z | W |
| A. | X位于元素周期表中第2周期、第VA族 | |
| B. | Y的氢化物(H2Y)不稳定,100℃以上即可分解 | |
| C. | W的非金属性比Y的非金属性弱 | |
| D. | Z的最高价氧化物的水化物是一种强碱 |
12.有关化学反应的方向和速率的研究可以指导化工生产.下列说法正确的是( )
| A. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3△H<0,在任何温度下均为自发反应 | |
| B. | 向新制氯水中加入少量小苏打固体可提高其漂白能力 | |
| C. | 1L密闭容器中发生反应4NH3+5O2?4NO+6H2O,充少量 N2可加快反应速率 | |
| D. | 湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu,反应中的Fe可以用Na代替 |
9.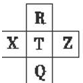 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 元素R对应气态氢化物的相对分子质量实际测量值往往比理论上要大的多,这可能和氢键有关 | |
| B. | 由于键能H-R>H-T,故元素R、T对应气态氢化物的沸点:HR>HT | |
| C. | R与Q的电子数相差16 | |
| D. | 最高价氧化物对应的水化物的酸性:X<T<Q |
10.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 明矾、漂白粉、臭氧的净水原理相同 | |
| B. | 硅胶可用作干燥剂 | |
| C. | 煤的干馏和石油的分馏都属于物理变化 | |
| D. | 亚硝酸钠是一种食品防腐剂,使用时其用量可以不加限制 |
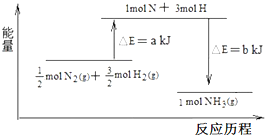 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.