题目内容
5.肼(N2H4)-空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%-30%的KOH溶液.电池总反应为:N2H4+O2═N2↑+2H2O.下列关于该燃料电池工作时的说法正确的是( )| A. | 溶液中阴离子物质的量基本不变 | |
| B. | 正极的电极反应式是:O2+4H++4e-═2H2O | |
| C. | 正极的电极反应式是:N2H4+4OH--4e-═H2O+N2↑ | |
| D. | 溶液中阴离子向正极移动 |
分析 该燃料电池中,负极上燃料失电子发生氧化反应,电极反应式为N2H4+4OH--4e═4H2O+N2↑,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-═4OH-,放电时,电解质溶液中阴离子向负极移动、阳离子向正极移动,据此分析解答.
解答 解:A.根据电池反应式知,KOH的物质的量在反应中不变,所以溶液中阴离子的物质的量基本不变,故A正确;
B.正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-═4OH-,故B错误;
C.正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-═4OH-,故C错误;
D.放电时,导致从负极沿导线流向正极,所以负极附近聚集大量阳离子,根据异性相吸原理,电解质溶液中阴离子向负极移动、阳离子向正极移动,故D错误;
故选A.
点评 本题考查化学电源新型电池,为高频考点,所有燃料电池中都是负极上燃料失电子、正极上氧化剂得电子,难点是电极反应式的书写,易错选项是B.

练习册系列答案
相关题目
15.下列化合物中不含离子键的是( )
| A. | Na2O | B. | HCl | C. | CaCl2 | D. | Na2CO3 |
13.PH3(膦)分子空间构型是三角锥形,以下关于PH3的叙述中,正确的是( )
| A. | PH3是非极性分子 | B. | PH3分子中的P-H 键是非极性键 | ||
| C. | PH3中心原子杂化轨道类型为sp2型 | D. | PH3分子中有未成键的电子对 |
20.下列说法不正确的是( )
| A. | 有机化合物中,σ键比π键重叠程度大,形成的共价键强 | |
| B. | N2H4分子中有5个σ键 | |
| C. | 气体单质中,一定有σ键,可能有π键 | |
| D. | 两种原子间形成共价键时,最多有一个σ键 |
10.在强酸性溶液中一定能大量共存的离子组是( )
| A. | OH-、Na+、K+、HCO3- | B. | Na+、K+、Cl-、Ag+ | ||
| C. | Mg+、SO42-、Na+、NO3- | D. | MnO4-、Fe2+、CO32-、Ba2+ |
17.A、B、C、D、E是元素周期表前四周期中的五种常见元素,其相关信息如下表:
请回答下列问题
(1)C元素原子的价电子排布图是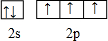
(2)E元素位于周期表ds区,E+离子的核外电子排布式是1s22s22p63s23p63d10
(3)CA3极易溶于水的主要原因是NH3与H2O分子间形成氢键C3-离子的中心原子采用sp杂化,C3-离子的空间构型是直线型
(4)A、C、E三种元素可形成〔E(CA3)4〕2+配离子,其中存在的化学键类型有①③(填序号,①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键)
(5)〔E(CA3)4〕2+可由E的硫酸盐溶液中通入过量CA3气体得到,写出该配离子的结构简式 .
.
| 元素 | 相关信息 |
| A | A原子的1S轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2P轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
(1)C元素原子的价电子排布图是

(2)E元素位于周期表ds区,E+离子的核外电子排布式是1s22s22p63s23p63d10
(3)CA3极易溶于水的主要原因是NH3与H2O分子间形成氢键C3-离子的中心原子采用sp杂化,C3-离子的空间构型是直线型
(4)A、C、E三种元素可形成〔E(CA3)4〕2+配离子,其中存在的化学键类型有①③(填序号,①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键)
(5)〔E(CA3)4〕2+可由E的硫酸盐溶液中通入过量CA3气体得到,写出该配离子的结构简式
 .
.
14.下列离子方程式属于盐的水解,且书写正确的是( )
| A. | NaHCO3溶液:HCO3-+H2O?CO32-+H3O+ | |
| B. | NaHS溶液:HS-+H2O?H2S+OH- | |
| C. | Na2CO3溶液:CO32-+2H2O?H2CO3+2OH- | |
| D. | Cl2溶于H2O中:Cl2+H2O═H++Cl-+HClO |
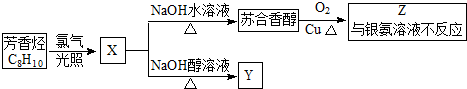
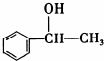 ,它不能发生的有机反应类型有④、⑥.
,它不能发生的有机反应类型有④、⑥.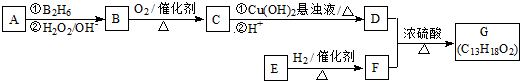
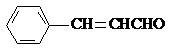 .
.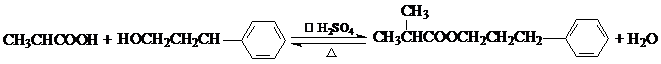 .
.