题目内容
【题目】过氧化钠与二氧化氮能发生反应,某兴趣小组对此进行探究,提出了两种假设。
假设一:Na2O2+2NO2===2NaNO2+O2↑
假设二:Na2O2+2NO2===2NaNO3
[查阅资料]
2NaNO2+2HCl===2NaCl+NO↑+NO2↑+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
[实验探究]
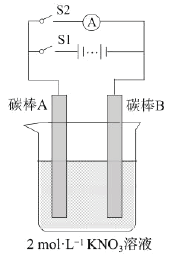
Ⅰ.按图示装置进行实验。
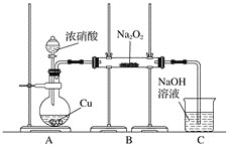
Ⅱ.通入二氧化氮至过氧化钠反应完全,然后对玻璃管中的固体物质进行检验。
[实验结论] 实验表明,过氧化钠与二氧化氮按“假设二”反应。
(1)过氧化钠与二氧化氮的反应中,氧化剂是____。
(2)装置A中反应的离子方程式是________。
(3)装置C的作用是__________。
(4)请设计实验证明装置B中的反应不符合“假设一”。
①实验操作:取玻璃管中的固体置于试管中,________;
②实验现象是________。
(5)有同学认为:只要直接观察C中导管口是否有气泡冒出,就可以判断B中的反应符合哪一种假设,这种想法________(填“对”或“不对”),原因是___________________。
【答案】过氧化钠 Cu+4H++2![]() =Cu2++2NO2↑+2H2O 吸收未充分反应的二氧化氮(或吸收尾气中的二氧化氮,防止污染空气) 向试管中加入适量盐酸 没有明显现象(或未见红棕色气体生成) 不对 若二氧化氮未充分反应,也可观察到C中导管口有气泡冒出
=Cu2++2NO2↑+2H2O 吸收未充分反应的二氧化氮(或吸收尾气中的二氧化氮,防止污染空气) 向试管中加入适量盐酸 没有明显现象(或未见红棕色气体生成) 不对 若二氧化氮未充分反应,也可观察到C中导管口有气泡冒出
【解析】
(1)过氧化钠与二氧化氮的反应中,过氧化钠中氧的化合价由-1价转化为-2价。
(2)装置A中,Cu与浓硝酸反应,生成Cu(NO3)2、NO2和H2O。
(3)因为NO2会污染环境,所以设计装置C。
(4)①实验操作:取玻璃管中的固体置于试管中,看是否有现象产生;
②从反应确定可能产生的实验现象。
(5)可从没有气体生成,是否也能产生气泡入手分析。
(1)过氧化钠与二氧化氮的反应中,过氧化钠中氧的化合价由-1价转化为-2价,则氧化剂是过氧化钠。答案为:过氧化钠;
(2)装置A中,Cu与浓硝酸反应,生成Cu(NO3)2、NO2和H2O,反应的离子方程式为Cu+4H++2![]() =Cu2++2NO2↑+2H2O。答案为:Cu+4H++2
=Cu2++2NO2↑+2H2O。答案为:Cu+4H++2![]() =Cu2++2NO2↑+2H2O;
=Cu2++2NO2↑+2H2O;
(3) 因为NO2是大气污染物,所以出现尾气处理装置,从而得出装置C的作用是吸收未充分反应的二氧化氮(或吸收尾气中的二氧化氮,防止污染空气)。答案为:吸收未充分反应的二氧化氮(或吸收尾气中的二氧化氮,防止污染空气);
(4)①从假设一的反应考虑设计实验,从而得出实验操作:取玻璃管中的固体置于试管中,向试管中加入适量盐酸;答案为:向试管中加入适量盐酸;
②产生的实验现象是没有明显现象(或未见红棕色气体生成);答案为:没有明显现象(或未见红棕色气体生成);
(5) 有同学认为:只要直接观察C中导管口是否有气泡冒出,就可以判断B中的反应符合哪一种假设,这种想法不对,原因是若二氧化氮未充分反应,也可观察到C中导管口有气泡冒出。答案为:不对;若二氧化氮未充分反应,也可观察到C中导管口有气泡冒出。

【题目】一定温度下,将1 mol X和3 mol Y置于2 L的恒容密闭容器中,发生反应:X(g)+3Y(g)2Z(g),反应过程中部分数据如表所示:
t/min | 0 | 10 | 20 | 30 | 40 |
p/kPa | 32 | 28.8 | 27.2 | 26.88 | 26.88 |
下列说法正确的是
A.10min时,用Y表示的平均反应速率为0.03 mol·L-1·min-1
B.X和Y的转化率之比保持不变时,可判断反应达到平衡状态
C.平衡状态时,c(Z)=0.32 mol·L-1
D.用气体分压代替物质的量浓度计算该反应的平衡常数,数值不变