题目内容
11.向体积为2L的固定密闭容器中通入3mol X气体,在一定温度下发生如下反应:2X(g)?Y(g)+3Z(g)(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为0.03mol•L-1•min-1.
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为甲:v(X)=3.5mol•L-1•min-1;乙:v(Y)=2mol•L-1•min-1;丙:v(Z)=4.5mol•L-1•min-1;丁:v (X)=0.075mol•L-1•s-1.若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)丁>乙>甲>丙.
(3)若向达到(1)的平衡体系中充入氮气,则平衡不(填“向左”“向右”或“不”)移动;若从达到(1)的平衡体系中移走部分Y气体,则平衡向右(填“向左”“向右”或“不”)移动.
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比较D
A.无法确定
B.前者一定大于后者
C.前者一定等于后者
D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,则:a、b、c应该满足的关系为c=3b,a≥0.
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为0.9<c≤4.5.
分析 (1)气体压强之比等于物质的量之比,结合化学平衡三段式列式计算Y的生成量,依据化学反应速率概念计算得到的;
(2)依据化学反应速率之比等于化学方程式中计量数之比,把四种情况下的反应速率化为一种物质表示的反应速率减小比较,温度越高反应速率越大
(3)体积不变平衡体系中充入氩气,平衡体系中各物质的浓度不变;向达到(1)的平衡体系中移走部分混合气体,气体的物质的量减小,相当于减小压强;
(4)若在相同条件下向I的平衡体系中再充入0.5mol X气体,相当于增大压强,平衡逆向进行,X的转化率减小;
(5)根据等效平衡建立的条件以及极限转化思想来回答;
(6)根据等效平衡,起始时维持化学反应向逆反应方向进行,说明c的数值大于达到平衡时Z的浓度,据此进行分析.
解答 解:由信息可知:2X(g)?Y(g)+3Z(g)
开始 3mol 0 0
转化 2x x 3x
平衡 3-2x x 3x
反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则$\frac{3-2x+x+3x}{3}$=1.2,解得x=0.3,
(1)Y的物质的量增加0.3mol,由v=$\frac{△c}{△t}=\frac{\frac{0.3mol}{2L}}{5min}$=0.03mol/(L.min),故答案为:0.03;
(2)将四个反应速率甲:ν(X)=3.5mol(L•min);乙:ν(Y)=2mol(L•min);丙:ν(Z)=4.5mol(L•min);丁:ν(X)=0.075mol(L•s),都统一到用X表示的反应速率值分别为甲:ν(X)=3.5mol(L•min);乙:ν(X)=4mol(L•min);丙:ν(X)=3mol(L•min);丁:ν(X)=4.5mol(L•min),所以化学反应速率是丁>乙>甲>丙,温度越高,化学反应速率越快,所以温度大小关系是:丁>乙>甲>丙,
故答案为:丁>乙>甲>丙;
(3)体积不变平衡体系中充入氩气,平衡体系中各物质的浓度不变,则平衡不移动;向达到(1)的平衡体系中移走部分混合气体,气体的物质的量减小,相当于减小压强,该反应为气体体积增大的反应,则平衡向右移动,
故答案为:不移动;向右;
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则体系压强增大,新平衡相当于是在原平衡基础上增大压强,逆向移动建立的,所以平衡后X的转化率减小;故答案为:D;
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达平衡时仍与(1)的平衡等效,根据极限转化结构以及等效的条件,需要等比即等效,即
2X(g)?Y(g)+3Z(g)
(1)的投料:3mol 0 0
等效投料:0 1.5mol 4.5mol,
现在投料:a b c
等效投料:0 0.5a+b 1.5a+c
所以 $\frac{b+0.5a}{1.5a+c}=\frac{1}{3}$,解得c=3b,且a≥0,故答案为:c=3b,a≥0;
(6)容器容积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,说明生成物Z浓度大于达到平衡时0.9mol;将3molX气体按照化学计量数全部转化为Z,c有最大值,最大值为4.5mol,所以c的范围为:0.9<c≤4.5,故答案为:0.9<c≤4.5.
点评 本题考查化学平衡的计算及平衡移动,把握达到平衡后压强与物质的量的变化为解答的关键,侧重分析能力、计算能力的考查,注意平衡计算的格式,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. |  向AgNO3和CuCl2的混合溶液中缓慢通入氨水溶液 | |
| B. |  向NaOH和Ca(OH)2的混合溶液中通入CO2 | |
| C. | 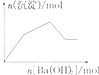 KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 | |
| D. | 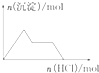 NaAlO2溶液中逐滴加入盐酸 |
| A. | 硅烷的分子通式可表示为SinH2n+2 | |
| B. | 甲硅烷燃烧生成二氧化硅和水 | |
| C. | 相同条件下甲硅烷(SiH4)的密度大于甲烷(CH4) | |
| D. | 甲硅烷的热稳定性强于甲烷 |
| A. | H2 | B. | NH3 | C. | KCl | D. | H2O |
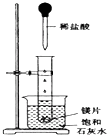 如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答:
如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答: 氯及其化合物在生产,生活中有着广泛的用途,回答下列问题:
氯及其化合物在生产,生活中有着广泛的用途,回答下列问题: