题目内容
20.下列物质含有离子键的是( )| A. | H2 | B. | NH3 | C. | KCl | D. | H2O |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属族元素、碱土金属族元素和氧族、卤族元素之间易形成离子键,据此分析解答.
解答 解:A.氢气分子中H-H原子之间存在共价键,故A错误;
B.氨气分子中N-H原子之间存在只存在共价键,故B错误;
C.氯化钾中钾离子和氯离子之间只存在离子键,故C正确;
D.水分子中H-O原子之间只存在共价键,故D错误;
故选C.
点评 本题考查离子键判断,侧重考查基本概念,把握物质构成微粒及微粒之间作用力即可解答,注意离子键和共价键的区别.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
(1)写出C原子的基态电子排布式[Ar]3d104s1.D中成对电子数与未成对电子数之比为2:1.
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点高(填“高”或“低”),其原因氨气分子之间存在氢键.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2为分子晶体,SiO2是原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,该配合物中存在的化学键类型是ABD.(填字母)
A、离子键 B、共价键 C、金属键 D、配位键 E、分子间作用力
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“O”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
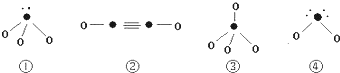
则在以上分子中,中心原子采用sp3杂化的是①③④;属于极性分子的是①④.(以上均填写序号).在②的分子中有3个σ键和2个π键.
| 元素 | A | B | C | D |
| 性质 结构 信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点高(填“高”或“低”),其原因氨气分子之间存在氢键.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2为分子晶体,SiO2是原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,该配合物中存在的化学键类型是ABD.(填字母)
A、离子键 B、共价键 C、金属键 D、配位键 E、分子间作用力
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“O”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
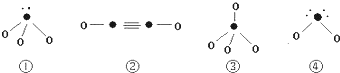
则在以上分子中,中心原子采用sp3杂化的是①③④;属于极性分子的是①④.(以上均填写序号).在②的分子中有3个σ键和2个π键.
8.下列有关海水提溴的叙述中,不正确的是( )
| A. | 利用空气吹出法提溴的过程为氯化→吹出→吸收 | |
| B. | 海水中的溴是以Br2形式存在,利用空气吹出法可获得Br2 | |
| C. | 吸收过程中,先用SO2将Br2还原为HBr,再用Cl2氧化HBr得到Br2 | |
| D. | 氯化过程发生的反应为2Br-+Cl2═Br2+2Cl- |
5.美国现任总统奥巴马就环境问题公开表示,到2020年,美国将会把温室气体排放量削减到1990年水平的80%,此外美国将把新能源比重提高到30%.奥巴马还计划每年拿出150亿美元大举投资太阳能、风能和生物质能等,并且举全国之力构建美国的低碳经济领袖地位.下列说法不正确的是( )
| A. | CO2、甲烷都属于温室气体 | |
| B. | 用甘蔗生产的燃料乙醇属可再生能源,利用乙醇燃料不会产生温室气体 | |
| C. | 太阳能、风能和生物质能属于新能源 | |
| D. | 太阳能电池可将太阳能直接转化为电能 |
9.下列三种有机物是某些药物中的有效成分
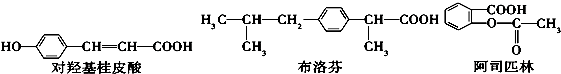
下列说法正确的是( )

下列说法正确的是( )
| A. | 三种有机物都是芳香烃 | |
| B. | 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 | |
| C. | 将等物质的量的三种物质加入NaOH溶液中,阿司匹林消耗NaOH最多 | |
| D. | 1 mol对羟基桂皮酸最多可以和2 mol NaHCO3反应 |
10.下列说法正确的是( )
| A. | 纸层析法分离Fe2+和Cu2+实验中滤纸作为惰性支持物,滤纸上吸附的水作为流动相 | |
| B. | 硫酸亚铁铵晶体过滤后用无水乙醇洗涤,阿司匹林晶体过滤后时用水洗 | |
| C. | 牙膏中的安息香酸钠、氟化钠等溶于水,水解使溶液显酸性 | |
| D. | 欲分离KNO3和NaCl按物质的量1:1组成的混合物,先将样品溶解,然后加热至表面出现晶膜后冷却,过滤得KNO3晶体;将母液加热至大量晶体析出后,用余热蒸干,得NaCl晶体 |