题目内容
18.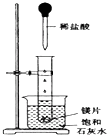 如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答:
如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列回答:(1)实验中能观察到的现象是ABD.(选填代号)
A.试管中镁片逐渐溶解 B.试管中产生无色气泡
C.烧杯外壁变冷 D.烧杯底部析出少量白色固体
(2)由实验推知,MgCl2溶液和H2的总能量小于(填“大于”“小于”“等于”)镁片和盐酸的总能量.
分析 如图所示的实验中,所试管内滴入稀盐酸,盐酸与镁剧烈反应放出氢气,同时反应放出的热量使饱和石灰水溶液温度升高,温度升高氢氧化钙溶解度减小,饱和溶液析出固体氢氧化钙而使溶液看上去变浑浊.
解答 解:(1)镁与盐酸剧烈反应,产生氢气并放出大量的热,由于氢氧化钙的溶解度随温度升高而减小,所以饱和石灰水升温后析出的氢氧化钙使溶液呈浑浊状,镁条溶解,故ABD选项中的现象符合;
故答案为:ABD;
(2)当反应物的能量高于生成物的能量时,反应是放热反应,故MgCl2溶液和H2的总能量小于镁片的盐酸的总能量,故答案为:小于.
点评 本题通过化学变化放热而使饱和溶液温度升高,此类本题之一巧;饱和溶液为溶解度随温度升高而减小的氢氧化钙的饱和溶液,此为本题又一巧;抓住二巧是解决问题的关键,题目较简单.

练习册系列答案
相关题目
9.下列表示式正确的是( )
| A. | 氨分子的电子式 | B. | 氢氧根离子的电子式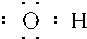 | ||
| C. | 乙酸的结构简式 C2H4O2 | D. | 苯的实验式 C6H6 |
13.乙炔在不同条件下可以转化成许多化合物(如图),下列叙述错误的是( )
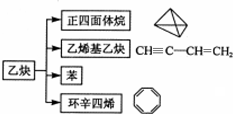

| A. | 图中五种有机物的实验式相同 | |
| B. | 乙炔生成乙烯基乙炔是加成反应 | |
| C. | 等质量的苯与乙烯基乙炔完全燃烧的耗氧量不同 | |
| D. | 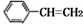 与环辛四烯均能使溴水褪色 与环辛四烯均能使溴水褪色 |
3.下列名词不是物理量专有名词的是( )
| A. | 时间 | B. | 物质的量 | C. | 质量 | D. | 摩尔 |
7.四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
(1)写出C原子的基态电子排布式[Ar]3d104s1.D中成对电子数与未成对电子数之比为2:1.
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点高(填“高”或“低”),其原因氨气分子之间存在氢键.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2为分子晶体,SiO2是原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,该配合物中存在的化学键类型是ABD.(填字母)
A、离子键 B、共价键 C、金属键 D、配位键 E、分子间作用力
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“O”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
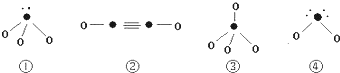
则在以上分子中,中心原子采用sp3杂化的是①③④;属于极性分子的是①④.(以上均填写序号).在②的分子中有3个σ键和2个π键.
| 元素 | A | B | C | D |
| 性质 结构 信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点高(填“高”或“低”),其原因氨气分子之间存在氢键.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2为分子晶体,SiO2是原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,该配合物中存在的化学键类型是ABD.(填字母)
A、离子键 B、共价键 C、金属键 D、配位键 E、分子间作用力
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“O”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
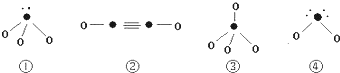
则在以上分子中,中心原子采用sp3杂化的是①③④;属于极性分子的是①④.(以上均填写序号).在②的分子中有3个σ键和2个π键.
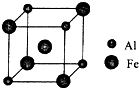 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.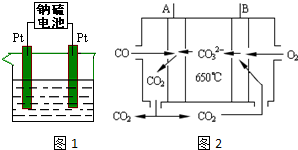
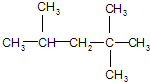 它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简
它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简 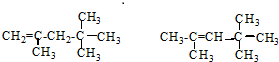 .
.