题目内容
15.20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性.X为n个C60连接而成的物质,结构如图: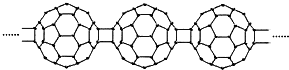
下列有关说法正确的是( )
| A. | C60转变为X是物理变化 | B. | X中含有极性共价键 | ||
| C. | X与金刚石互为同素异形体 | D. | X能够发生加成反应 |
分析 A.化学变化有新物质生成;
B.不同非金属元素之间形成的化学键为极性共价键;
C.由同种元素组成的不同种单质互称为这种元素的同素异形体;
D.每个碳原子成四个键,该物质含有双键.
解答 解:A.C60转变为X,有新物质生成,属于化学变化,故A错误;
B.X为n个C60连接而成的物质,X中只含有非极性共价键,故B错误;
C.C60是碳元素的一种单质,与金刚石、石墨互为同素异形体,故C正确;
D.因为该物质含有双键,一定条件下X可发生加成反应,故D正确.
故选CD.
点评 本题考查有机物的结构与性质、物理变化、化学键等,难度不大,注意C60是单质,不是化合物.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
5.已知16S和34Se位于同一主族,下列说法正确的是( )
| A. | 热稳定性:H2Se>H2S>H2O | B. | 原子半径:Se>S>Cl | ||
| C. | 酸性:H2SeO4>H2SO4>HClO4 | D. | 还原性:S2->Se2->Br- |
6.关于乙烯分子中的共价键,下列描述正确的是( )
| A. | 含有5个σ键、1个π键 | |
| B. | C-H之间是碳的sp2杂化轨道与H的s轨道形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键 | |
| C. | 只有sp2杂化轨道才形成π键 | |
| D. | C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形的σ键 |
3.仅用下表提供的仪器和用品能够实现相应目的是( )
| 选项 | 实验目的 | 仪器和用品 |
| A | 分离乙醇和乙酸乙酯的混合物 | 分液漏斗、烧杯、玻璃棒 |
| B | 检验溶液中是否含有SO42- | 试管、胶头滴管、Ba(NO3)2 |
| C | SO2既有氧化性,又有还原性 | 试管、胶头滴管、氯水、品红 |
| D | 配制100mLpH=2的盐酸 | 100mL容量瓶、烧杯、玻璃棒、胶头滴管、酸式滴定管、pH=1的盐酸 |
| A. | A | B. | B | C. | C | D. | D |
7.体积相同的甲乙两个容器中,分别充有等物质的量的SO2、O2,甲容器保持体积不变,乙容器保持压强不变,在相同温度下,发生2SO2(g)+O2(g)?2SO3(g)并达到平衡.则下列说法不正确的是( )
| A. | 平均反应速度:乙>甲 | B. | 平衡时SO3的物质的量甲>乙 | ||
| C. | 平衡时SO2的转化率:乙>甲 | D. | 平衡时混合气体的密度甲<乙 |
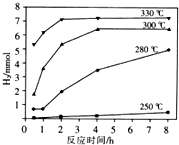 天然气的主要成分是甲烷,含有少量的羰基硫(COS)、乙硫醇(C2H5SH)等气体.
天然气的主要成分是甲烷,含有少量的羰基硫(COS)、乙硫醇(C2H5SH)等气体. .
.
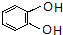 ,C的系统命名是3-溴丙烯(或3-溴-1-丙烯).
,C的系统命名是3-溴丙烯(或3-溴-1-丙烯).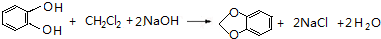 (或
(或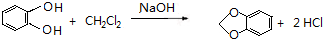 ).
).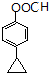 或
或 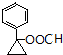 (任写一种).
(任写一种).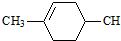 ═CHCOOCH2CH=CHCH2OOCH═
═CHCOOCH2CH=CHCH2OOCH═
 +
+ →
→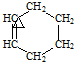
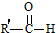 +
+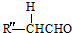 $→_{△}^{OH-}$R′CH
$→_{△}^{OH-}$R′CH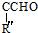 +H2O
+H2O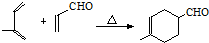 .
.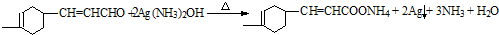 .
.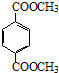 .
.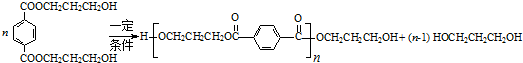 .
.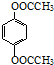 (邻、间、对三种中的任一种).
(邻、间、对三种中的任一种).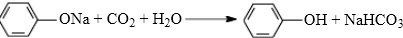 .
.