题目内容
6.关于乙烯分子中的共价键,下列描述正确的是( )| A. | 含有5个σ键、1个π键 | |
| B. | C-H之间是碳的sp2杂化轨道与H的s轨道形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键 | |
| C. | 只有sp2杂化轨道才形成π键 | |
| D. | C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形的σ键 |
分析 A.单键为σ键,双键中有1个σ键和1个π键;
B.C与C之间是sp2杂化轨道形成的一个σ键和未参加杂化的2p轨道形成的π键;
C.C与C之间未参加杂化的2p轨道形成π键;
D.C与C之间有1个σ键和1个π键.
解答 解:A.乙烯分子中存在4个C-Hσ键,1个C-Cσ键和1个π键,则分子中含有5个σ键、1个π键,故A正确;
B.C-H之间是s轨道与sp2轨道形成的σ键,C与C之间是sp2杂化轨道形成的一个σ键和未参加杂化的2p轨道形成的π键,故B错误;
C.C与C之间未参加杂化的2p轨道形成π键,故C错误;
D.C与C之间有1个σ键和1个π键,则C与C之间是sp2杂化轨道形成的一个σ键和未参加杂化的2p轨道形成的π键,故D错误;
故选A.
点评 本题考查共价键的类型及杂化轨道,侧重分子结构与性质的考查,注意双键中的π键及杂化轨道不能形成π键为解答的关键,题目难度中等.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
16.下列变化过程中破坏化学键的是( )
| A. | 水加热汽化 | B. | 熔融氯化钠 | C. | 乙醇溶于水 | D. | 粉碎金刚石 |
17.下列各组中的反应,属于同一反应类型的是( )
| A. | 由2-溴丙烷制2-丙醇;由丙烯与水反应制丙醇 | |
| B. | 由甲苯制对硝基甲苯;由甲苯制苯甲酸 | |
| C. | 由氯代环己烷制环己烯;由丙烯与溴水反应制1,2-二溴丙烷 | |
| D. | 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯与水反应制苯甲酸和乙醇 |
14.汽车尾气中的二氧化氮在低层大气中可形成化学烟雾,并循环生成臭氧,反应机理为:( )
①NO2$\frac{\underline{\;he\;}}{\;}$NO+O;②O+O2═O;③-----.该过程的总反应为3O2═2O3.则下列说法正确的是.
①NO2$\frac{\underline{\;he\;}}{\;}$NO+O;②O+O2═O;③-----.该过程的总反应为3O2═2O3.则下列说法正确的是.
| A. | 反应③为N2O4═2NO2 | |
| B. | 该过程最终会导致大气中O的含量增加 | |
| C. | 总反应中NO2作催化剂 | |
| D. | 该反应可用于修复大气“臭氧空调” |
1.下列有关电子排布图的表述正确的是( )
| A. | 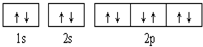 可表示单核10电子粒子基态时电子排布 可表示单核10电子粒子基态时电子排布 | |
| B. | 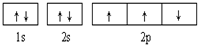 此图错误,违背了泡利原理 此图错误,违背了泡利原理 | |
| C. | 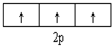 表示基态N原子的价电子排布 表示基态N原子的价电子排布 | |
| D. |  表示处于激发态的B的电子排布图 表示处于激发态的B的电子排布图 |
11.下列各组分子中,都属于含极性键的非极性分子的是( )
| A. | C2F4 CH3Cl | B. | CO2 C2H2 | C. | C60 S8 | D. | NH3 PH3 |
15.20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性.X为n个C60连接而成的物质,结构如图:
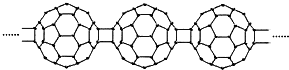
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | C60转变为X是物理变化 | B. | X中含有极性共价键 | ||
| C. | X与金刚石互为同素异形体 | D. | X能够发生加成反应 |
16.下列有关σ键、π键的说法错误的是( )
| A. | 一般碳碳σ键比π键重叠程度大,形成的共价键强 | |
| B. | 分子中含有共价键,则至少含有一个σ键 | |
| C. | 在气体单质中,一定有σ键,可能有π键 | |
| D. | CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C-H σ键 |
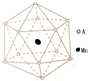 准晶体亦称为准晶或拟晶,是一种介于晶体和非晶体之间的固体结构.
准晶体亦称为准晶或拟晶,是一种介于晶体和非晶体之间的固体结构.