题目内容
7.实验室测得4mol SO2参加下列反应:2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ•mol-1.当放出354kJ热量时SO2转化率最接近于( )| A. | 10% | B. | 30% | C. | 50% | D. | 90% |
分析 热化学方程式2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ•mol-1表示通常条件下2molSO2(g)、1molO2(g)反应生成2molSO3(g)放出热量196.6kJ,根据物质的量与热量成正比,依据热化学方程式定量关系求出参加反应的二氧化硫的物质的量,再根据转化率的等于计算SO2的转化率.
解答 解:2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ•mol-1.
2mol 196.6KJ
n 354kJ
n=$\frac{2mol×354kJ}{196.6kJ}$=3.60mol,
SO2的转化率=$\frac{3.60mol}{4mol}$×100%=90%,故选D.
点评 本题考查了热化学方程式的计算分析,注意热化学方程式的含义是解题的关键,题目较简单.

练习册系列答案
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
13.反应2C(s)+O2(g)=2CO(g) 的能量变化如图所示,下列说法正确的是( )

| A. | 生成物的总能量大于反应物的总能量 | |
| B. | △H<0,表明该反应在常温下一定能发生 | |
| C. | 2 mol C(s)与足量O2(g)反应生成CO2(g),放出的热量大于221 kJ | |
| D. | 该反应的热化学方程式是:2C(s)+O2(g)=2CO(g)△H=-110.5 kJ/mol |
14.已知反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,当转移6mol电子时,被还原的HNO3的物质的量为( )
| A. | 8mol | B. | 4mol | C. | 2mol | D. | 6mol |
2.下列装置或操作能达到实验目的是( )
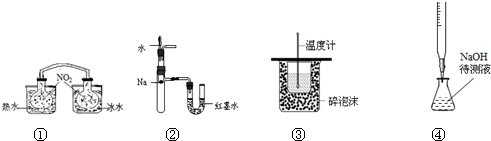

| A. | 装置①依据两容器内气体颜色变化,判断反应2NO2(g)?N2O4(g)平衡移动的方向 | |
| B. | 装置②依据反应后U管两边液面的高低,判断Na和水反应的热效应 | |
| C. | 装置③测定稀强酸与稀强碱反应的中和热 | |
| D. | 装置④用标准的盐酸溶液滴定待测的氢氧化钠溶液(部分加持仪器略去) |
12.在100℃和200kPa的条件下,密闭容器中进行的化学反应aA(g)?bB(g)+cC(g)达到平衡状态,在维持体系温度不变的条件下逐步压缩体积,体系压强也逐渐增大,测定不同压强下反应再次建立平衡时物质B的浓度,结果如表所示.
根据表中的数据,回答下列问题(提示:温度和压强的改变可能会对物质的聚集状态产生影响)
(1)压强从200kPa增加到500kPa时,平衡不移动(填“正向”或“逆向”或“不”),理由是浓度增大的倍数和压强增大的倍数相同.
(2)压强从500kPa增加到1000kPa时,平衡正向移动(填“正向”或“逆向”或“不”),其原因可能为加压至1000kPa时,C物质变成了非气态物质.
(3)化学方程式中的化学计量数的关系是:a=b+c(填“?”“?”或“?”)
| 压强(kPa) | 200 | 500 | 1000 |
| B的浓度(mol/L) | 0.04 | 0.1 | 0.27 |
(1)压强从200kPa增加到500kPa时,平衡不移动(填“正向”或“逆向”或“不”),理由是浓度增大的倍数和压强增大的倍数相同.
(2)压强从500kPa增加到1000kPa时,平衡正向移动(填“正向”或“逆向”或“不”),其原因可能为加压至1000kPa时,C物质变成了非气态物质.
(3)化学方程式中的化学计量数的关系是:a=b+c(填“?”“?”或“?”)
19.对于淀粉和纤维素的叙述,正确的是( )
| A. | 因为都是多糖,所以都有甜味 | |
| B. | 因为具有相同的分子式(C6H10H5)n,所以互为同分异构体 | |
| C. | 两者都能水解为葡萄糖 | |
| D. | 两者都是人类的营养食物 |
16.下列对摩尔的叙述中不正确的是( )
| A. | 摩尔是一个单位,用于计量物质所含微观粒子的数量 | |
| B. | 摩尔是一个物理量 | |
| C. | 1mol任何气体所含的气体分子数目都相等 | |
| D. | 摩尔既能用来计量纯净物,又能用来计量混合物 |
17.放置于空气中,易发生氧化还原反应而变质的物质( )
| A. | Na2O2 | B. | NaHCO3 | C. | Na | D. | NaOH |
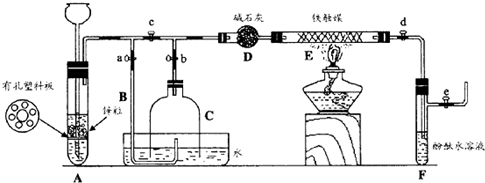
 2NH3.
2NH3.