题目内容
16.下列对摩尔的叙述中不正确的是( )| A. | 摩尔是一个单位,用于计量物质所含微观粒子的数量 | |
| B. | 摩尔是一个物理量 | |
| C. | 1mol任何气体所含的气体分子数目都相等 | |
| D. | 摩尔既能用来计量纯净物,又能用来计量混合物 |
分析 摩尔是物质的量的单位,用于计量物质含有微观粒子,使用物质的量必须指明具体的物质或微粒,可以是单一物质,也可以是混合物,每摩尔微粒含有阿伏伽德罗常数个微粒.
解答 解:A、摩尔是物质的量的单位,用于计量物质含有微观粒子,故A正确;
B、摩尔是物质的量的单位,不是物理量,故B错误;
C、1mol任何气体所含的气体分子数都是阿伏伽德罗常数,故C正确;
D、摩尔可以用来计量纯净物,也可以用来计量混合物,故D正确,
故选B.
点评 本题主要考查的是学生对于摩尔这一概念的理解,比较基础,注意基础知识的理解掌握.

练习册系列答案
相关题目
7.实验室测得4mol SO2参加下列反应:2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ•mol-1.当放出354kJ热量时SO2转化率最接近于( )
| A. | 10% | B. | 30% | C. | 50% | D. | 90% |
11.室温下,某一元碱A与0.01mol/L某一元强酸等体积混合后所得溶液的pH为7.下列说法中正确的是( )
①若A为强碱,其溶液的物质的量浓度等于0.01mol/L
②若A为弱碱,其溶液的物质的量浓度大于0.01mol/L
③反应前,A溶液中c(OH-)一定是0.01mol/L
④反应后,混合溶液中阴离子的总浓度大于阳离子的总浓度.
①若A为强碱,其溶液的物质的量浓度等于0.01mol/L
②若A为弱碱,其溶液的物质的量浓度大于0.01mol/L
③反应前,A溶液中c(OH-)一定是0.01mol/L
④反应后,混合溶液中阴离子的总浓度大于阳离子的总浓度.
| A. | ①② | B. | ③④ | C. | ①②③ | D. | ①②③④ |
8.除去括号内杂质所用试剂和方法不正确的是( )
| A. | Cu(Fe)--溶于足量盐酸,过滤 | B. | KNO3(NaCl)--结晶 | ||
| C. | 水(NaCl)--蒸馏 | D. | CO2(HCl)--氢氧化钠溶液,洗气 |
5.下列粒具有相同的质子数和电子数的是( )
| A. | OH-、H2O、F- | B. | NH3、NH4+、F- | C. | H3O+、NH4+、Cl- | D. | HCl、F2、H2S |
6.下列关于钠的说法正确的是( )
| A. | 钠是活泼的非金属 | B. | 钠与水反应放出氧气 | ||
| C. | 钠与水反应放出氢气 | D. | 钠不与盐酸反应 |

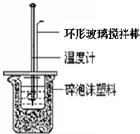 “中和热的测定”实验步骤为:
“中和热的测定”实验步骤为: