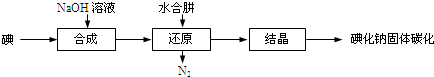
题目内容
2.下列装置或操作能达到实验目的是( )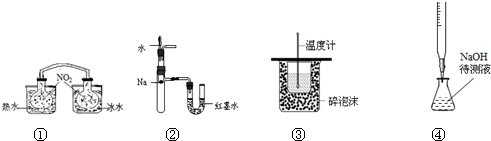
| A. | 装置①依据两容器内气体颜色变化,判断反应2NO2(g)?N2O4(g)平衡移动的方向 | |
| B. | 装置②依据反应后U管两边液面的高低,判断Na和水反应的热效应 | |
| C. | 装置③测定稀强酸与稀强碱反应的中和热 | |
| D. | 装置④用标准的盐酸溶液滴定待测的氢氧化钠溶液(部分加持仪器略去) |
分析 A.N2O4是红棕色气体,放入热水中,平衡逆向移动,放入冷水中平衡正向移动;
B.钠与反应放热,大试管内气体受热膨胀;
C.缺少搅拌器;
D.盐酸应用酸式滴定管.
解答 解:A.反应2NO2(g)?N2O4(g)为放热反应,放入热水中,平衡逆向移动,二氧化氮的浓度增大,颜色加深;放入冷水中,平衡正向移动,二氧化氮浓度减小,颜色变浅,所以能实现实验目的,故A正确;
B.钠与反应放热,大试管内气体受热膨胀,U管左侧液面下降,右侧液面上升,所以能实现实验目的,故B正确;
C.装置③测定中和热,缺少搅拌器,导致测量不准确,故C错误;
D.盐酸应用酸式滴定管,不能用碱式滴定管,故D错误.
故选AB.
点评 本题考查化学实验方案评价,侧重考查基本操作、基本原理,明确实验原理是解本题关键,注意从装置的目的性、操作的准确性等方面评价,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
8.下列有机物中,属于糖类的是( )
| A. | 油脂 | B. | 淀粉 | C. | 酒精 | D. | 蛋白质 |
9.下列说法正确的是( )
| A. | 金属甲的阳离子比同价态的金属乙的阳离子氧化性强,则金属甲比金属乙活泼 | |
| B. | 原电池中电子从负极经过溶液流向正极 | |
| C. | 电解池中电解质溶液的阳离子向阴极迁移 | |
| D. | 在铁制品上镀银,铁做正极,银做负极 |
7.实验室测得4mol SO2参加下列反应:2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ•mol-1.当放出354kJ热量时SO2转化率最接近于( )
| A. | 10% | B. | 30% | C. | 50% | D. | 90% |
14.废旧印刷电路板的回收利用科实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是BD.
A.热裂解形成燃油
B.露天焚烧
C.作为有机复合建筑材料的原料
D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=64.39kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.84kJ•mol-1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1.
(3)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol•L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见表).
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是H2O2分解速率加快.
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+.
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是BD.
A.热裂解形成燃油
B.露天焚烧
C.作为有机复合建筑材料的原料
D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=64.39kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.84kJ•mol-1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1.
(3)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol•L-1H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见表).
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率(10-3mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
(4)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+.
11.室温下,某一元碱A与0.01mol/L某一元强酸等体积混合后所得溶液的pH为7.下列说法中正确的是( )
①若A为强碱,其溶液的物质的量浓度等于0.01mol/L
②若A为弱碱,其溶液的物质的量浓度大于0.01mol/L
③反应前,A溶液中c(OH-)一定是0.01mol/L
④反应后,混合溶液中阴离子的总浓度大于阳离子的总浓度.
①若A为强碱,其溶液的物质的量浓度等于0.01mol/L
②若A为弱碱,其溶液的物质的量浓度大于0.01mol/L
③反应前,A溶液中c(OH-)一定是0.01mol/L
④反应后,混合溶液中阴离子的总浓度大于阳离子的总浓度.
| A. | ①② | B. | ③④ | C. | ①②③ | D. | ①②③④ |
12.据最新报道,科学家发现了如下反应:O2+PtF6═O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt的化合价为+5,对于此反应,下列说法正确的是( )
| A. | 在此反应中,O2是氧化剂,PtF6是还原剂 | |
| B. | O2(PtF6)中氧元素的化合价为+1 | |
| C. | O2(PtF6)只是氧化产物 | |
| D. | 每生成1molO2(PtF6)则转移1mol电子 |