题目内容
(10分)可逆反应aA(g) + bB(g) cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。

试比较下列大小关系:T1 T2, P1 P2, ΔH 0,ΔS 0。 使用催化剂的是 反应线。
 cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
试比较下列大小关系:T1 T2, P1 P2, ΔH 0,ΔS 0。 使用催化剂的是 反应线。
<;<;<;>;甲
试题分析:根据图像A可知,曲线T2首先达到平衡状态,温度高反应速率快,到达平衡的时间少,所以T1<T2;根据图像B可知,曲线P2首先达到平衡状态,压强高反应速率快,到达平衡的时间少,所以P1<P2;根据图像A可知,温度越高C的含量越低,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应,即△H<0;根据图像B可知,压强越高C的含量越低,这说明增大压强平衡向逆反应方向移动,因此正方应是体积增大的可逆反应,所以△S>0;催化剂只能改变反应速率而不能改变平衡状态,所以使用催化剂的是甲反应线。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
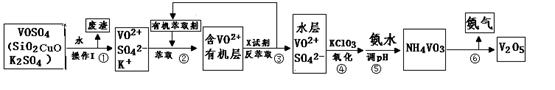
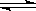 VOM2(有机层) + H2SO4 (水层)
VOM2(有机层) + H2SO4 (水层) 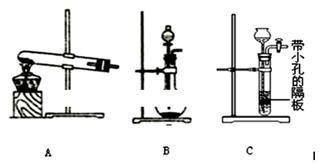
 2NH3一定处于平衡状态的是……… ( )
2NH3一定处于平衡状态的是……… ( ) B+C(g)-Q达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是
B+C(g)-Q达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析正确的是 CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。 2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是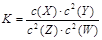 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是 2Z(g) + 2W(g)
2Z(g) + 2W(g) I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法中不正确的是
I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法中不正确的是 