��Ŀ����
13��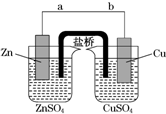 ijѧ��������ͼʵ��װ��̽������ʽԭ��صĹ���ԭ����CuԪ�ص����ԭ������Ϊ64��������ʵ�鲽�����λش��������⣺
ijѧ��������ͼʵ��װ��̽������ʽԭ��صĹ���ԭ����CuԪ�ص����ԭ������Ϊ64��������ʵ�鲽�����λش��������⣺��1�������е�������Ϊa��b����a��b��ʾ����
��2����װ����ͭ�缫����������0.64g��������ת�Ƶĵ�����ĿΪ0.02NA �� ���á�NA����ʾ��
��3��װ���������г�������֬�⣬��Ҫ����KCl�ı�����Һ����ع���ʱ���������е�K+��Cl-���ƶ�����ı�����ȷ����B��
A�������е�K+������ձ��ƶ���Cl-���Ҳ��ձ��ƶ�
B�������е�K+���Ҳ��ձ��ƶ���Cl-������ձ��ƶ�
C�������е�K+��Cl-��������ձ��ƶ�
D�������е�K+��Cl-���������ƶ�
��4��������Ӧ2Fe3++Cu�TCu2++2Fe2+��Ƴ�ԭ��أ�д���缫��Ӧʽ��������Ӧ2Fe3++2e-=2Fe2+��
��5���������û�ѧ����ʽ��ʾ�Ļ�ѧ�仯������ÿС���ĺ�����ע��������ת����ʽ��
�ٵ���ܷ�Ӧ��Zn+Ag2O+H2O�TZn��OH��2+2Ag����ѧ��ת��Ϊ���ܣ�
��2C2H2+5O2$\stackrel{��ȼ}{��}$4CO2+2H2O����ѧ��ת��Ϊ���ܣ�
��6H2O+6CO2$��_{Ҷ����}^{��}$C6H12O6�������ǣ�+6O2��̫���ܣ����ܣ�ת��Ϊ��ѧ�ܣ�
���� ��1�����ݽ����������ж���������ԭ����У������ɸ�������������
��2�����ݵ缫��Ӧʽ������ؼ��㣬�ó���ȷ���ۣ�
��3�������������ж��������ӵ��ƶ�����
��4���ɷ���ʽ��֪��Cu��������Ϊԭ��صĸ�������������Ϊ̼������Cu���õĽ������������ҺΪ�Ȼ�����Һ������������ԭ��Ӧ����������������Ӧ���ݴ˷������
��5���ӷ�Ӧ�������ж�������ת����ʽ��
��� �⣺��1��пͭԭ����У�п��ͭ���ã���пΪ������ͭΪ������ԭ����У������ɸ��������������ʵ��ӵ�����Ϊa��b���ʴ�Ϊ��a��b��
��2��0.64gͭ���ʵ���Ϊ0.01mol���ɵ缫��ӦʽCu2++2e-=Cu��֪������1molͭ��ת��2mol���ӣ�������0.01molͭ��������ת��0.02mol���ӣ�������ĿΪ0.02NA���ʴ�Ϊ��0.02NA ��
��3������ձ���пʧ���ӱ��п���ӣ�ʹ��п�缫����������ɣ�����������������ձ��ƶ����Ҳ��ձ���ͭ���ӵõ����ӱ��ͭ��ʹ��ͭ�缫����������ɣ��������������Ҳ��ձ��ƶ����������е�K+���Ҳ��ձ��ƶ���Cl-������ձ��ƶ����ʴ�Ϊ��B
��4���ɷ���ʽ2Fe3++Cu�TCu2++2Fe2+��֪��Cu��������Ϊԭ��صĸ�����������ӦΪCu-2e-=Cu2+������Fe3+����ԭ���缫����ʽΪ2Fe3++2e-=2Fe2+���ʴ�Ϊ��2Fe3++2e-=2Fe2+��
��5���ٷŵ���ͨ��ԭ���װ�ðѻ�ѧ��ת��Ϊ���ܣ��ʴ�Ϊ����ѧ��ת��Ϊ���ܣ�
��ȼ���Ǿ��ҵ�������ԭ��Ӧ���ѻ�ѧ��ת��Ϊ���ܣ��ʴ�Ϊ����ѧ��ת��Ϊ���ܣ�
����ɫֲ����Ҷ�����ڣ����պ����ù��ܰѶ�����̼��ˮ�ϳ������ǣ�ͬʱ�ų��������ʴ�Ϊ��̫���ܣ����ܣ�ת��Ϊ��ѧ�ܣ�
���� ������Ҫ������ԭ�����ơ�����ԭ�������ʵ�������ؼ��㡢����������ת����ʽ����ȷԭ���ԭ���ǽⱾ��ؼ����ٸ��ݷ���ʽ��Ԫ�ػ��ϼ۱仯ȷ�����������ϼ��������Һ��ͬʱ����ѧ���������⡢����������������Ŀ�Ѷ��еȣ�

| A�� | ����ˮ���𱽡����Ȼ�̼������ϩ | |
| B�� | ��ȥ�����������ӣ��ȼ�Ũ��ˮ���ٹ��� | |
| C�� | �����Ը��������Һϴ�������Գ�ȥ������������ϩ | |
| D�� | ��ȥ���������е�������Ҵ���������������Һϴ�ӣ��ٷ�Һ |
| A�� | Al3+ Na+NO3- Cl- | B�� | K+ Na+Cl- NO3- | ||
| C�� | K+ Na+ Cl-AlO2- | D�� | K+ NH4+ SO42-NO3- |
| A�� | ��״���£�0.1molCl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA | |
| B�� | ���³�ѹ�£�44 g C3H8�к��е�̼̼������Ϊ3 NA | |
| C�� | 6.4 gͭ����������۳�ַ�Ӧ��ʧȥ�ĵ�����Ϊ0.2 NA | |
| D�� | 1 mol Na2O��Na2O2�����������������������3 NA |
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
| A�� | ��ѧ��Ӧ�е������仯����Ҫ���ɻ�ѧ���ı仯����� | |
| B�� | ���ڿ��淴Ӧ��aA��g��+bB��g���TbC��g��+dD��g�����������Ӧ�Ƿ��ȷ�Ӧ���淴Ӧһ�������ȷ�Ӧ | |
| C�� | ����ȼ������ˮ��һ�����ȷ�Ӧ��˵��1mol H2����������1mol H2O������ | |
| D�� | ���Ȳ��ܷ����ķ�Ӧ����һ�������ȷ�Ӧ |
 �� O22+�ЦҼ���Ŀ�ͦм���Ŀ֮��Ϊ1��2��
�� O22+�ЦҼ���Ŀ�ͦм���Ŀ֮��Ϊ1��2��
 ��
��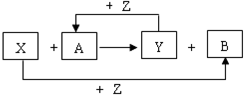 X��Y��ZΪ���������ֵ��ʣ�Z����ɫֲ�������õIJ���֮һ��A��BΪ���������������һ�������¿ɷ�����ͼ��ʾ�ķ�Ӧ�������ڷ���Һ�н��еķ�Ӧ����
X��Y��ZΪ���������ֵ��ʣ�Z����ɫֲ�������õIJ���֮һ��A��BΪ���������������һ�������¿ɷ�����ͼ��ʾ�ķ�Ӧ�������ڷ���Һ�н��еķ�Ӧ����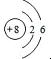 ��
�� ��
�� ��
��