题目内容
【题目】废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(主要成分为Cu、Zn)制备CuSO4·5H2O的部分实验步骤如图:
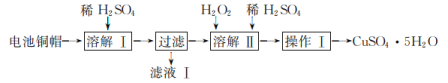
下列说法错误的是( )
A.“溶解I”中,为加快溶解速率,可将铜帽粉碎
B.“滤液I”中,溶质的主要成分为ZnSO4
C.“溶解II”过程中,有大量的气体产生
D.“操作I”需要用到酒精灯玻璃棒等仪器
【答案】C
【解析】
废旧电池的铜帽(主要成分为Cu、Zn)加入稀硫酸溶解,铜不与硫酸反应,锌与硫酸反应生成可溶性盐硫酸锌,则“滤液I”中溶质的主要成分为ZnSO4,滤渣为Cu,滤渣中加入双氧水和稀硫酸,酸性条件下,双氧水可氧化铜,发生反应为:Cu+H2O2+H2SO4= CuSO4+2H2O,得到硫酸铜溶液,再经过蒸发浓缩、冷却结晶、过滤操作得到CuSO4·5H2O,据此分析解答。
A.为将铜帽粉碎,增大与稀硫酸的接触面积,可加快溶解速率,故A正确;
B.“溶解I”中,铜不与硫酸反应,锌与硫酸反应生成可溶性盐硫酸锌,则“滤液I”中溶质的主要成分为ZnSO4,故B正确;
C.“溶解II”过程中,酸性条件下,双氧水可氧化铜,发生反应为:Cu+H2O2+H2SO4= CuSO4+2H2O,反应过程中没有气体产生,故C错误;
D.“操作I”包括蒸发浓缩、冷却结晶、过滤,需要用到酒精灯玻璃棒等仪器,故D正确;
答案选C。

【题目】脱硝技术是处理氮氧化物的有效方法之一。在1L的恒容密闭容器中充入2mol NH3、1mol NO和1mol NO2,发生反应:2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g)△H。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:
2N2(g)+3H2O(g)△H。在不同温度下发生上述反应,测得N2的物质的量(mol)与时间的关系如下表:
0 | 10 min | 20 min | 30 min | 40 min | |
T1K | 0 | 0.6 | 1.1 | 1.5 | 1.5 |
T2K | 0 | 0.8 | 1.4 | 1.4 | 1.4 |
回答下列问题:
(1)上述反应中___________(填字母)。
A. △S>0,△H>0 B. △S>0,△H<0 C. △S<0,△H>0 D. △S<0,△H<0
(2)T1_______(填“>”“<”或“=”)T2,理由是___________________________________________
(3)T1K下,0~20min内v(NO)=______________
(4)T2K下,NO2的平衡转化率为_____________