��Ŀ����
����Ŀ���±���Ԫ�����ڱ���һ���֡�
����������Ԫ�������ڱ��е�λ�ã��ش������й����⣺�����û�ѧ������д��
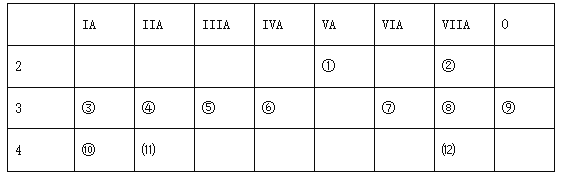
��1��д������Ԫ�ط��ţ��� ���� ��
��2������ЩԪ�ص�����������Ӧˮ�����У�������ǿ���� ��������ǿ���� �������Ե����������� �����û�ѧʽ��д��
��3������ЩԪ���е��ʵ���������ǿ���� ����ԭ����ǿ���� ����ѧ��������õ�Ԫ���� �����û�ѧʽ��д��
��4������ԭ�ӽṹʾ��ͼ���� ��
��5���õ���ʽ��ʾ�������γɻ�����Ĺ��̣� ��
��6���������ֱ��γɵ���̬�⻯��Ļ�ѧʽ�� �� ��������Բ��ȶ����� ��
��7�����������У���ѧ���ʽϻ��õ��� ������Ԫ�ط��ţ�
���������У���ѧ���ʽϻ��õ��� ������Ԫ�ط��ţ����֤���������ӷ���ʽ��ʾ����
��
���𰸡���1��N Si
��2��HClO4��KOH��Al��OH��3
��3����2��K��Ar
��4��![]()
��5��![]()
��6��H2S ��HCl��H2S
��7��Na��Cl�� Cl2+ 2Br-==Br2 + 2Cl-
���������������������Ԫ�����ڱ���Ԫ���٢ڢۢܢݢޢߢ���(11)(12)�ֱ���N��F��Na��Mg��Al��Si��S��Cl��Ar��K��Ca��Br����1��Ԫ�ط��ţ���N����Si��
��2���ǽ�����Խǿ����������Ӧˮ��������Խǿ����û�к����ᣬ����������ǿ����HClO4��������Խǿ����������Ӧˮ�������Խǿ����������ǿ����KOH�������Ե�����������Al(OH)3
��3���ǽ�����Խǿ������Խǿ�����ʵ���������ǿ���ǣ�2��������Խǿ��ԭ��Խǿ����ԭ����ǿ����K��ϡ�����廯ѧ��������ã�����õ�Ԫ����Ar��
��4��Caԭ�ӽṹʾ��ͼ��![]() ��
��
��5���õ���ʽ��ʾK��S�γ�K2S�Ĺ��̣�![]()
��6���ǽ�����Խǿ��̬�⻯��Խ�ȶ���S��Cl�ֱ��γɵ���̬�⻯��Ļ�ѧʽ��H2S��HCl��������Բ��ȶ�����H2S��
��7����Na��Mg�У���ѧ���ʽϻ��õ���Na
��Cl��Br�У���ѧ���ʽϻ��õ���Cl��Cl2+ 2Br-==Br2 + 2Cl-��֤����ѧ���ʽϻ��õ���Cl��

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�