题目内容
【题目】某化学研究性学习小组针对原电池形成条件,设计了实验方案,进行如下探究。
(1)请填写有关实验现象并得出相关结论。
编号 | 实验装置 | 实验现象 |
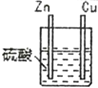
1 |
| 锌棒逐渐溶解,表面有气体生成;铜棒表面无现象 |
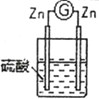
2 |
| 两锌棒逐渐溶解,表面均有气体生成;电流计指针不偏转 |
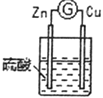
3 |
| 铜棒表面的现象是______________________,电流计指针___________________ |
①通过实验2和3,可得出原电池的形成条件是______________________________。
②通过实验1和3,可得出原电池的形成条件是______________________________。
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,从而可得出原电池形成条件是___________________。
(2)分别写出实验3中Zn棒和Cu棒上发生的电极反应式:
Zn棒:______________________________。
Cu棒:______________________________。
(3)实验3的电流是从________棒流出(填“Zn”或“Cu”),反应过程中若有0.4mol电子发生了转移,则Zn电极质量减轻___________g。
【答案】有气体生成 发生偏转 活泼性不同的两个电极 形成闭合回路 有电解质溶液 Zn-2e-=Zn2+ 2H++2e-=H2↑ Cu 13
【解析】
(1)根据实验现象、装置特点结合原电池的构成条件、原电池工作原理分析解答;
(2)实验3中锌是负极,铜是正极,据此解答。
(3)原电池中电流与电子的流向相反,根据负极反应式计算。
(1)实验3中构成原电池,锌是负极,铜是正极,溶液中的氢离子放电,则铜棒表面的现象是有气体生成,电流计指针发生偏转;
①实验2和3相比电极不一样,因此可得出原电池的形成条件是有活泼性不同的两个电极。
②实验1和3相比实验3中构成闭合回路,由此可得出原电池的形成条件是形成闭合回路。
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,由于乙醇是非电解质,硫酸是电解质,因此可得出原电池形成条件是有电解质溶液。
(2)锌是负极,发生失去电子的氧化反应,则Zn棒上发生的电极反应式为Zn-2e-=Zn2+。铜是正极,溶液中的氢离子放电,则Cu棒上发生的电极反应式为2H++2e-=H2↑。
(3)实验3中锌是负极,铜是正极,则电流是从Cu棒流出,反应过程中若有0.4mol电子发生了转移,根据Zn-2e-=Zn2+可知消耗0.2mol锌,则Zn电极质量减轻0.2mol×65g/mol=13.0g。

 名校课堂系列答案
名校课堂系列答案【题目】
(1)I.已知:Na2S2O3 + H2 SO4=Na2SO4 + SO2↑+S↓+H2O,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
①该实验①、②可探究温度对反应速率的影响,因此V1= , V2 = , V3=;
(2)②若V4=10.0,V5=6.0,则实验①、③可探究 对反应速率的影响。
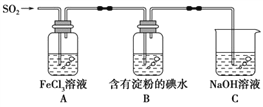
(3)Ⅱ.利用反应:I2+2Na2S2O3=Na2S4O6+2NaI可定量测定硫代硫酸钠(Mr=158)的纯度,现在称取wg硫代硫酸钠固体样品,配成250 mL的溶液,取25.00 mL置于锥形瓶中,加入指示剂,用a mol/L的碘水滴定,消耗碘水b mL,则:
①滴定应选择的指示剂是 , 滴定终点的现象为。
②对于该滴定实验的有关操作或误差分析正确的是。
A.滴定前,要用对应装入的溶液润洗滴定管和锥形瓶
B.滴定过程中,标准液滴到锥形瓶外,会使所测得的结果偏大
C.滴定开始时滴定管尖嘴有气泡,滴定结束后气泡消失,测得纯度将偏小
D.滴定前仰视读数而滴定结束时俯视读数,则所测得的纯度将会偏小
③样品中硫代硫酸钠纯度的表达式为。