题目内容
8.下列化学用语正确的是( )| A. | 三氟化氮的电子式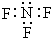 | B. | 水合氢离子电子式: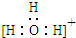 | ||
| C. | 氟离子的结构示意图: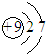 | D. | 中子数为18的硫原子${\;}_{16}^{34}$S |
分析 A.漏掉了氟原子的1对未成键孤对电子;
B.水合氢离子中O原子还含有一个孤电子对;
C.氟离子的核电荷数为9,核外电子总数为10,最外层为8个电子;
D.质量数=质子数+中子数,元素符号的左上角表示质量数、左下角表示质子数.
解答 解:A.三氟化氮分子中,氮原子和氟原子最外层都达到8电子稳定结构,其正确的电子式为: ,故A错误;
,故A错误;
B.水合氢离子中O原子还含有一个孤电子对,其电子式为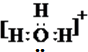 ,故B错误;
,故B错误;
C.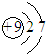 为氟原子,氟离子的核外电子总数为10,氟离子正确的结构示意图为:
为氟原子,氟离子的核外电子总数为10,氟离子正确的结构示意图为: ,故C错误;
,故C错误;
D.硫元素的质子数为16,中子数为18的硫原子的质量数为34,该原子可以表示为:${\;}_{16}^{34}$S,故D正确;
故选D.
点评 本题考查了常见化学用语的判断,题目难度中等,注意掌握离子结构示意图、电子式、元素符号等化学用语的概念及书写原则,明确离子结构示意图与原子结构示意图、离子化合物与共价化合物的电子式的区别,试题培养了学生规范答题的能力.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
16.将11.2g铁粉加入250mL 2mol/L氯化铁溶液中充分反应后,结果是( )
| A. | 铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变 | |
| B. | 往溶液中滴入无色KSCN溶液,溶液变红色 | |
| C. | Fe2+和Fe3+物质的量之比为5:1 | |
| D. | 氧化产物和还原产物的物质的量之比为2:5 |
13.A气体的水溶液呈酸性,若将A通入酸性的KMnO4溶液中,则紫红色褪色;若将A通入Br2水中,则Br2褪色并出现浑浊,则A气体是( )
| A. | Cl2 | B. | SO2 | C. | H2S | D. | CO2 |
20.下列对一些实验事实和理论解释正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | Na与水反应失去1个电子,Mg与水反应失去2个电子 | Na的金属性比Mg强 |
| B | 氢溴酸的酸性强于盐酸的酸性 | Br的非金属性比Cl强 |
| C | K3C60在熔融状态下能够导电 | K3C60中含有离子键 |
| D | HF的沸点高于HCl | F的非金属性比Cl强 |
| A. | A | B. | B | C. | C | D. | D |
18.在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质①FeCl3,②Fe2O3,③Cu(NO3)2,④KNO3,
铜粉溶解的是( )
铜粉溶解的是( )
| A. | 只有①或② | B. | 只有②或④ | C. | 只有①或②或③ | D. | 上述物质均可 |