题目内容
【题目】某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如下图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如下图乙所示。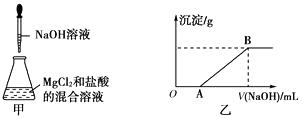
请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有(填字母)。
a.天平 b.烧杯
c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为。
(3)AB段反应的离子方程式为。
(4)在B点对应的溶液中滴加AgNO3溶液,观察到的现象是 , 反应的离子方程式为。
【答案】
(1)bd
(2)H++OH?=H2O
(3))Mg2++2OH?=Mg(OH)2↓
(4)有白色沉淀生成,Ag++Cl?=AgCl↓
【解析】乙图中OA段表明OH先与H+反应,AB段为OH与Mg2+反应,B点对应溶液为NaCl溶液,加入AgNO3溶液发生反应:Ag++Cl=AgCl↓。
(1)根据固体化学物质的溶解操作判断需要的仪器;
(2)混合物中氢离子首先与氢氧根离子发生中和反应;
(3)氢离子反应完后镁离子与氢氧根离子反应生成氢氧化镁沉淀;
(4)溶液中的铝离子与银离子反应生成氯化银沉淀.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
【题目】某同学在实验室中进行如下实验:
编号 | Ⅰ | Ⅱ | Ⅲ |
实验 |
|
|
|
现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
以下结论正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为CuCl2
C.Ⅲ中的离子方程式为2H++Zn=Zn2++H2↑
D.Ⅲ中发生的反应不是离子反应