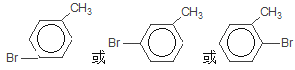
题目内容
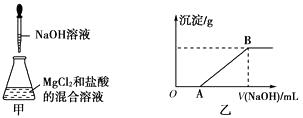
【题目】某同学在实验室中进行如下实验:
编号 | Ⅰ | Ⅱ | Ⅲ |
实验 |
|
|
|
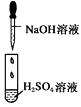
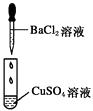
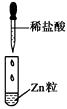
现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
以下结论正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为CuCl2
C.Ⅲ中的离子方程式为2H++Zn=Zn2++H2↑
D.Ⅲ中发生的反应不是离子反应
【答案】C
【解析】Ⅰ中虽无明显现象,但发生了离子反应:H++OH-=H2O,A项不符合题意;
Ⅱ中发生反应为:Ba2++SO42-=BaSO4↓,白色沉淀为BaSO4,B项不符合题意;
Ⅲ中的反应是离子反应,离子方程式为Zn+2H+=Zn2++H2↑,C项符合题意,D项不符合题意。
故答案为:C
根据发生的离子反应进行判断实验现象、书写离子方程式即可.

练习册系列答案
相关题目
【题目】根据实验内容填空:
(1)甲同学利用下列装置来进行铜跟浓硫酸反应实验. 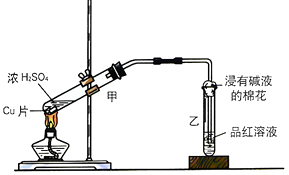
①写出甲装置中发生的主要反应的化学方程式 .
②乙同学认为,若要用铜制取硫酸铜,可以先用铜和氧气反应生成氧化铜,然后利用氧化铜和稀硫酸反应可以得到硫酸铜.若要制取硫酸铜,请你从环境保护和节约资源的角度分析,比较甲同学和乙同学制取硫酸铜的方法中更合理的是 , 原因是 . 
(2)丙同学利用下图的方法实验室制取并验证SO2某些性质,并将实验情况记录在表中,请完成以下表格:
装置序号 | 实验现象或作用 | 实验结论或化学方程式 |
① | 有气泡产生 | 化学方程式为: |
② | 紫色石蕊试液变色 | 证明SO2溶于水显酸性 |
③ | 品红溶液褪色 | 证明SO2具有性 |
④ | 溶液变浑浊 | 证明SO2具有性 |
⑤ | 溴水褪色 | 证明SO2具有性 |
⑥ | 吸收尾气 | 证明SO2属于性氧化物 |