题目内容
8.有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、NO3-、SO42-、Cl-、HCO3-、SO32-、Cu2+,取该溶液实验如下:①取少量该溶液,加几滴石蕊试液,溶液变红色
②取少量该溶液,适当浓缩,加Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色
③取少量该溶液,加BaCl2溶液,有白色沉淀生成
④取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3
⑤取少量该溶液,加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解
根据上述实验现象判断:
(1)溶液中肯定存在的离子是Mg2+、Al3+、NO3-、SO42-.
(2)溶液中肯定不存在的离子是Fe2+、HCO3-、SO32-、Cu2+.
(3)不能确定的离子是Na+、Cl-,为进一步确定可能存在的离子,应该补充的实验是①用焰色反应来判断Na+、②再另取少量该溶液,往其中滴加足量的Ba(NO3)2溶液后,取上层澄清液少许,往其中滴加含HNO3的AgNO3溶液,看是否有白色沉淀生成,来判断是否含Cl-.
分析 依据溶液无色,可排除有色的Fe2+、Cu2+;①加几滴石蕊试液,溶液变红色,数目溶液呈酸性,则一定不存在CO3-;
②Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色,该气体为二氧化氮,则一定存在NO3-;
③加BaCl2溶液,有白色沉淀生成,白色沉淀为硫酸钡,则一定含有SO42-或SO32-;
④取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3,不能确定是否含Cl-;
⑤加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解,确定含有Mg2+、Al3+,则一定不存在HCO3-、SO32-,据此进行解答.
解答 解:因为是无色透明溶液,Fe2+是浅绿色、Cu2+是蓝色,故原溶液中一定不存在Fe2+、Cu2+;
①取少量该溶液,加几滴石蕊试液,溶液变红色,说明溶液显酸性,故一定不含HCO3-;
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色,无色气体是NO,红色气体为NO2,故溶液中存在NO3-;
③取少量该溶液,加BaCl2溶液,有白色沉淀生成,故溶液中含有SO42-或SO32-;
④取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3不能确定是否含有Cl-,因为③中引入了氯离子;
⑤取少量该溶液,加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解,镁离子与铝离子都生成沉淀,沉淀部分溶解,即氢氧化铝溶解,氢氧化镁不溶,故一定含有 Mg2+、Al3+,根据离子共存则一定不存在HCO3-、SO32-,结合③可知一定存在SO42-,
(1)依据以上分析,溶液中一定存在的离子是:Mg2+、Al3+、NO3-、SO42-,
故答案为:Mg2+、Al3+、NO3-、SO42-;
(2)依据以上分析,溶液中一定不存在的离子是:Fe2+、HCO3-、SO32-、Cu2+,
故答案为:Fe2+、HCO3-、SO32-、Cu2+;
(3)不能确定是否存在的离子是Na+、Cl-,为进一步确定可能存在的离子,应该补充的实验是:①用焰色反应来判断Na+、②再另取少量该溶液,往其中滴加足量的Ba(NO3)2溶液后,取上层澄清液少许,往其中滴加含HNO3的AgNO3溶液,看是否有白色沉淀生成,来判断是否含Cl-,
故答案为:Na+、Cl-;①用焰色反应来判断Na+、②再另取少量该溶液,往其中滴加足量的Ba(NO3)2溶液后,取上层澄清液少许,往其中滴加含HNO3的AgNO3溶液,看是否有白色沉淀生成,来判断是否含Cl-.
点评 本题考查常见离子的检验,题目难度中等,熟练掌握常见离子的性质及检验方法为解答关键,注意明确检验离子是否存在是,必须排除干扰离子,如③中引入了氯离子,则④中无法判断原溶液中是否含有氯离子.

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案| A. | 负极反应:H2-2e-═2 H+ | |
| B. | 通O2的一极是发生还原反应 | |
| C. | 工作一段时间后电解质溶液的c(OH-)增大 | |
| D. | 工作时负极区附近pH增大 |
| A. | 化学反应必伴随能量变化 | |
| B. | 反应是放热还是吸热须看反应物和生成物具有的总能量的相对大小 | |
| C. | Ba(OH)2•8H2O和NH4Cl(固体)混合搅拌发生的是吸热反应 | |
| D. | 燃煤发电不需经过其它能量转换过程,可直接把化学能转化为电能 |
| A. | 反应所生成的气体体积:a杯>b杯 | B. | 反应所需要的时间:a杯>b杯 | ||
| C. | 刚开始时反应的速率:b杯>a杯 | D. | 整个反应阶段平均速率:a杯>b杯 |
| A. | 食物放在冰箱里 | B. | 在糕点包装内放置小包除氧剂 | ||
| C. | 燃煤发电时用煤粉代替煤块 | D. | 塑料制品中添加抑制剂 |
| A. | 它可作耐磨材料 | |
| B. | 它不可用作致冷剂 | |
| C. | 晶体中每个碳原子形成2个碳氧双键 | |
| D. | 晶体中碳、氧原子个数之比为1:2 |
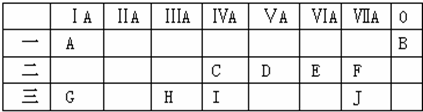
 ,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.
,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.