题目内容
4.表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ).| 物质 | Cl2 | Br2 | I2 | H2 | HF | HCl HBr HI |
| 能量 | 243 | 193 | 151 | 436 | 568 | 432 366 298 |
(1)下列物质本身具有的能量最低的是A (填A.B.C.D)
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中,最稳定的是A (填A.B.C.D)
A.HF B.HCl C.HBr D.HI
(3)X2+H2=2HX(X代表Cl、Br、I)的反应是放热反应(填“吸热”或“放热”)
(4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是Cl2(填写分子式).
(5)若无上表中的数据,你能正确回答出问题(4)吗?能.(填能、否)你的根据是元素的非金属性越强,生成物越稳定,放出的热量越多,在这几种HX中,HCl最稳定,放出的热量多.
分析 (1)破坏1mol 物质中的化学键所消耗的能量越高则说明物质越稳定,物质具有的能量越低;
(2)根据破坏1 mol物质中的化学键所消耗的能量越大,则物质越稳定;
(3)形成新键释放的热量和旧键断裂吸收的热量多少判断;
(4)相同条件下,等物质的量的X2(卤素单质)分别与足量的氢气反应,依据键能计算分析判断;
(5)依据同主族元素非金属性越强,氢化物越稳定,能量越低,放出的热量越多解答.
解答 解:(1)根据表中数据可知,破坏1molCl2中的化学键所消耗的能量为234KJ,破坏1molBr2中的化学键所消耗的能量为193KJ,破坏1molI2中的化学键所消耗的能量为151KJ,破坏1molH2中的化学键所消耗的能量为436KJ,所以破坏1mol 氢气消耗能量最高,氢气最稳定,能量最低;
故选:A;
(2)根据表中数据可知,破坏1mol氯化氢中的化学键所消耗的能量最高,则说明HF最稳定;
故选:A;
(3)根据反应X2+H2═2HX,新键生成释放的热量按照HCl、HBr、HI顺序分别是:432×2=864kJ、366×2=732kJ、298kJ×2=596kJ,旧键断裂吸收的热量的热量按照HCl、HBr、HI顺序分别是243+436=679kJ、193+436=629kJ、151+436=587kJ,所以新键生成释放的能量均大于旧键断裂吸收的热量,所以X2+H2═2HX的反应是放热反应,
故答案为:放热;
(4)根据表中数据可知,破坏1mol物质中的化学键所消耗的能量越高,生成物越稳定,发生该反应放出的热量越多,故答案为:Cl2;
(5)若无上表中的数据,能正确回答出问题(4),因为,Cl、Br、I为同主族元素,依据同主族元素性质递变规律可知,Cl、Br、I非金属性依次减弱,非金属性越强,与氢气化合越容易,反应放出热量越多,生成的氢化物越稳定;
故答案为:能;元素的非金属性越强,生成物越稳定,放出的热量越多,在这几种HX中,HCl最稳定,放出的热量多.
点评 本题考查了化学键与反应物稳定性的关系,明确键能大小与物质的稳定性关系是解题关键,题目难度不大.

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案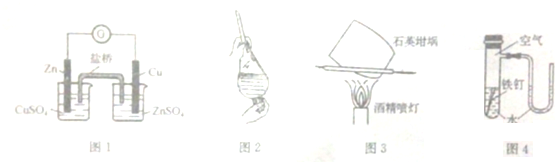
| A. | 用图1装置构成锌--铜原电池 | |
| B. | 用图2装置选择裂化汽油提取溴水中溴 | |
| C. | 用图3装置灼烧碳酸钙制取少量氧化钙 | |
| D. | 用图4装置验证在该条件下铁钉发生吸氧腐蚀 |
| A. | 只有碳、氢两种元素组成的有机化合物称为烃 | |
| B. | 乙醛和乙酸都含有碳氧双键,二者都能发生加成反应 | |
| C. | 苯可以发生加成反应,但苯中不含有碳碳双键 | |
| D. | 乙醇和苯酚都含有羟基都能发生酯化反应 |
| A. | KOH | B. | NH3 | C. | H2O | D. | CaCl2 |
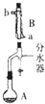 实验室用乙酸和正丁醇制备乙酸正丁酯的反应如下
实验室用乙酸和正丁醇制备乙酸正丁酯的反应如下CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
物质的相关数据如下表:
| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
①在干燥的50ml圆底烧瓶中,加入3.7g的正丁醇和3.3g冰醋酸,再加入2~3滴浓硫酸,摇匀,投入1~2粒沸石 按图安装带分水器的回流反应装置,并在分水器中预先加入水,使水面略低于分水器的支管口.打开冷凝水,圆底烧瓶在石棉网上用小火加热.在反应过程中,通过分水器下部的旋塞不断分出生成的水,注意保持分水器中水层液面原来的高度,使油层尽量回到圆底烧瓶中.反应达到终点后,停止加热,记录分出的水的体积.
(二)产品的精制
②将分水器分出的酯层和反应液一起倒入分液漏斗中,用适量的水洗涤.有机层继续用一定体积10%Na2CO3洗涤至中性,再用适量的水洗涤,最后将有机层转移至锥形瓶中,再加入少量无水硫酸镁固体.静置片刻,过滤除去硫酸镁固体.
③将②处理后的乙酸正丁酯滤入50 mL 烧瓶中,进行蒸馏纯化,收集126.1℃的馏分,得乙酸正丁酯3.5g.
回答有关问题:
(1)装置B的名称是球形冷凝管
(2)步骤①中判断反应终点的依据是分水器中的水层不再增加时,视为反应的终点
(3)产品的精制过程步骤②中,第一次水洗的目的是洗去大部分的硫酸和醋酸等用饱和Na2CO3溶液洗涤有机层,该操作的目的是除去产品中含有的残留酸等杂质第二次洗的目的是洗去乙酸正丁酯中的盐分实验中加入少量无水硫酸镁的目的是干燥
(4)下列关于蒸馏操作的说法,正确的是B
A、温度计的水银柱应插入到液面以下
B、蒸馏过程中,加入沸石(碎瓷片)的目的是防止暴沸
C、冷凝管进出水的方向是上进下出
D、为提高蒸馏的速度,可以不用石棉网而直接用酒精灯进行加热.
(5)步骤③的常压蒸馏,需收126.1℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是防止因温差过大,冷凝管炸裂
(6)该实验过程中,列式计算生成乙酸正丁酯的产率(保留2位有效数字)60%.
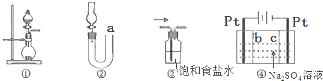
| A. | 图①可用于实验室制取少量NH3或O2 | |
| B. | 可用从a处加水的方法检验图②装置的气密性 | |
| C. | 实验室可用图③的方法除去Cl2中混有的HCl | |
| D. | 利用图④装置制硫酸和氢氧化钠,其中b为阳离子交换膜 |
| A. | 可根据同周期元素的第一电离能变化规律,推出Al的第一电离能比Mg大 | |
| B. | 结构和组成相似的分子晶体,沸点随相对分子质量增大而升高,推出NH3的沸点低于PH3 | |
| C. | 根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 | |
| D. | 根据溶解度小的沉淀易向溶解度更小的沉淀转化的规律,推出在ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
| A. | X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有12mol σ键 | |
| B. | Z的最高价含氧酸分子中,羟基氧和非羟基氧个数比为1:1 | |
| C. | Y的气态氢化物分子中H-Y-H键角比Y的最高价氧化物分子中O-Y-O键角小 | |
| D. | Z的气态氢化物比Y的气态氢化物稳定,是因为氢键的影响 |
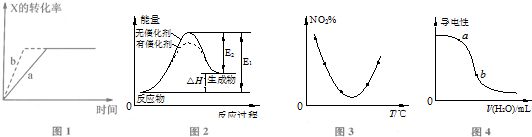
| A. | 图1所示反应:X(g)+2Y(g)?3Z(g),b曲线表示的一定是增大压强 | |
| B. | 图2表示催化剂能改变化学反应的焓变 | |
| C. | 图3表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)═N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 | |
| D. | 图3表示向稀CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |