题目内容
2.X、Y为两种短周期元素,其原子的最外层电子数分别是1和6,则X、Y两种元素形成的常见化合物或者离子不可能是( )| A. | 只含极性键的共价化合物 | |
| B. | 含非极性键的共价化合物 | |
| C. | 阴阳离子个数之比为1:1的离子化合物 | |
| D. | 可形成双核离子或者四核离子 |
分析 X、Y为两种短周期元素,其原子的最外层电子数分别为1和6,则X处于ⅠA族、Y处于ⅥA族,结合两族元素形成常见物质及构成微粒对各选项 进行判断.
解答 解:X、Y为两种短周期元素,其原子的最外层电子数分别为1和6,则X处于ⅠA族、Y处于ⅥA族,
A.H与O、S形成的水、硫化氢分子中只含极性键,故A错误;
B.H与氧元素写出的双氧水分子中含有O-O非极性键,且属于共价化合物,故B错误;
C.ⅠA族与ⅥA族元素不能形成阴阳离子个数之比为1:1的离子化合物,故C正确;
D.H、O元素可以形成双核离子OH-和四核离子H3O+,故D错误,
故选C.
点评 本题考查了位置、结构与性质关系的应用,题目难度中等,熟练掌握原子结构与元素周期律、元素周期律的关系为解答关键,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列反应中是吸热反应的是( )
| A. | 氧化钙溶于水 | B. | 乙醇燃烧 | ||
| C. | 铝粉与氧化铁粉末反应 | D. | 碳酸钙受热分解 |
8. 铅蓄电池是常用的汽车电池.其结构如图所示.铅蓄电池以铅板为负极,表面蒙有大量二氧化铅的铅板作正极,以适当浓度的H2SO4作电解质溶液.已知PbSO4不溶于水也不溶于H2SO4.此电池放电的原理与普通原电池相同,充电时则相当于电解池.下列关于铅蓄电池的说法中正确的是( )
铅蓄电池是常用的汽车电池.其结构如图所示.铅蓄电池以铅板为负极,表面蒙有大量二氧化铅的铅板作正极,以适当浓度的H2SO4作电解质溶液.已知PbSO4不溶于水也不溶于H2SO4.此电池放电的原理与普通原电池相同,充电时则相当于电解池.下列关于铅蓄电池的说法中正确的是( )
 铅蓄电池是常用的汽车电池.其结构如图所示.铅蓄电池以铅板为负极,表面蒙有大量二氧化铅的铅板作正极,以适当浓度的H2SO4作电解质溶液.已知PbSO4不溶于水也不溶于H2SO4.此电池放电的原理与普通原电池相同,充电时则相当于电解池.下列关于铅蓄电池的说法中正确的是( )
铅蓄电池是常用的汽车电池.其结构如图所示.铅蓄电池以铅板为负极,表面蒙有大量二氧化铅的铅板作正极,以适当浓度的H2SO4作电解质溶液.已知PbSO4不溶于水也不溶于H2SO4.此电池放电的原理与普通原电池相同,充电时则相当于电解池.下列关于铅蓄电池的说法中正确的是( )| A. | 放电时,负极质量减小,正极质量增大 | |
| B. | 放电时,当电路中通过2mol e-时,消耗2mol H2SO4 | |
| C. | 放电时,溶液中SO${\;}_{4}^{2-}$向正极区移动 | |
| D. | 放电时,整个电解质溶液的pH逐渐变大 |
12.下列化合物中,熔沸点最高的是( )
| A. | NaCl | B. | MgCl2 | C. | NaBr | D. | NaI |
14.已知:H2O(g)=H2O(l)△H=Q1 kJ/mol
C2H5OH(g)═C2H5OH(l)△H=Q2 kJ/mol
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=Q3kJ/mol
若使46克酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
C2H5OH(g)═C2H5OH(l)△H=Q2 kJ/mol
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=Q3kJ/mol
若使46克酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
| A. | ( Q1+Q2+Q3 ) kJ | B. | 0.5( Q1+Q2+Q3 ) kJ | ||
| C. | ( 0.5Q1-1.5Q2+0.5Q3 ) kJ | D. | ( 3Q1-Q2+Q3 ) kJ |
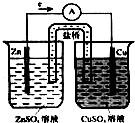 如图是铜锌原电池,又称丹尼尔电池.请回答:
如图是铜锌原电池,又称丹尼尔电池.请回答: .
.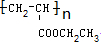 .
.