题目内容
14.已知:H2O(g)=H2O(l)△H=Q1 kJ/molC2H5OH(g)═C2H5OH(l)△H=Q2 kJ/mol
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=Q3kJ/mol
若使46克酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
| A. | ( Q1+Q2+Q3 ) kJ | B. | 0.5( Q1+Q2+Q3 ) kJ | ||
| C. | ( 0.5Q1-1.5Q2+0.5Q3 ) kJ | D. | ( 3Q1-Q2+Q3 ) kJ |
分析 利用已知的反应计算出C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)的反应热△H,利用乙醇的物质的量与反应放出的热量成正比来解答.
解答 解:①H2O(g)═H2O(l)△H1=Q1kJ•mol-1,
②C2H5OH(g)═C2H5OH(l)△H2=Q2kJ•mol-1,
③C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H3=Q3kJ•mol-1,
根据盖斯定律可知,①×3+③-②得C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l),故△H=(3Q1+Q3-Q2)kJ/mol,
46g酒精液体为1mol,故1mol液态乙醇完全燃烧并恢复至室温,则放出的热量为( 3Q1-Q2+Q3 ) kJ,
故选D.
点评 本题考查学生利用盖斯定律计算反应热,题目难度中等,根据已知热化学方程式构造目标热化学方程式是关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.如图所示,下列叙述正确的是( )
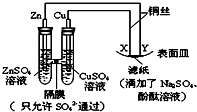

| A. | Y为阴极,发生还原反应 | B. | X为正极,发生氧化反应 | ||
| C. | 锌电极表面有红色的铜析出 | D. | X与滤纸接触处变红 |
20.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,16g O2和32g O3的混合物中,含有O原子数目为3NA | |
| B. | 标准状态下,1mol Na2O和1mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1mol NaHSO4溶于水或受热熔化,电离出来的离子数目均为2NA | |
| D. | 在K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O中,若生成71g Cl2,转移的电子数目为$\frac{5}{3}$NA |
2.X、Y为两种短周期元素,其原子的最外层电子数分别是1和6,则X、Y两种元素形成的常见化合物或者离子不可能是( )
| A. | 只含极性键的共价化合物 | |
| B. | 含非极性键的共价化合物 | |
| C. | 阴阳离子个数之比为1:1的离子化合物 | |
| D. | 可形成双核离子或者四核离子 |
9.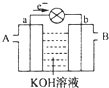 如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
 如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )| A. | a电极发生还原反应,b电极发生氧化反应 | |
| B. | a电极的电极反应式为:CO+4OH-+2e-=CO2+2H2O | |
| C. | A处通入的是空气,B处通入的是CO | |
| D. | 用这种电池作电源精炼铜,若阴极质量增加6.4 g,则至少消耗标准状况下的CO 2.24 L |
6.某食品包装袋上的说明如下:
以下说法不正确的是( )
| 品名 | 苏打饼干 |
| 配料 | 面料、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、苏打 |
| 保质期 | 12个月 |
| 生产日期 | 2015年5月15日 |
| A. | 精炼食用植物油能使溴水和酸性KMnO4溶液褪色 | |
| B. | 白砂糖属于二糖,在人体内水解而转化为单糖 | |
| C. | 鲜鸡蛋清遇浓硝酸变为黄色 | |
| D. | 奶油与白砂糖都是高分子化合物 |
3.下列有关电化学原理的说法错误的是( )
| A. | 可充电的电池称“二次电池”,在充电时,是将电能装化为化学能,在放电时,又将化学能转化为电能 | |
| B. | 在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 | |
| C. | 对于冶炼像钠、钙、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法 | |
| D. | 氯化铝的熔点比氧化铝低,因此工业上最好采用电解熔融氯化铝来制备单质铝 |
4.下列说法不正确的是( )
| A. | 丁烷有2种同分异构体,它们的物理和化学性质都不相同 | |
| B. | 在一定条件下,苯与液溴、硝酸作用生成溴苯、硝基苯的反应都属于取代反应 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物( 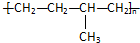 )可由单体CH3CH=CH2和CH2=CH2加聚制得 )可由单体CH3CH=CH2和CH2=CH2加聚制得 |
 ;
;