题目内容
研究化肥的合成、废水的处理等有现实的重要意义.
Ⅰ.尿素是一种非常重要的高氮化肥,工业上合成尿素的反应如下:
2NH3(l)+CO2(g)?H2O(l)+H2NCONH2(l)△H=-103.7kJ?mol-1
试回答下列问题:
(1)下列措施中有利于提高尿素的产率的是 .
A.采用高温 B.采用高压 C.寻找更高效的催化剂
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)?H2NCOONH4(氨基甲酸铵)(l)△H1
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(l)△H2
某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
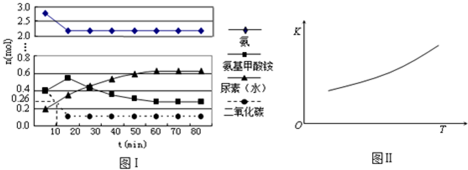
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定.
②反应进行到10min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)= .
③第二步反应的平衡常数K随温度的变化如图Ⅱ所示,则△H20 (填“>”“<”或“=”).
Ⅱ.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表.
工厂污染物排放浓度及允许排放标准
几种砷酸盐的Ksp
回答以下问题:
(3)若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol?L-1,c(AsO43-)最大是 mol?L-1.
(4)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 .
(5)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降.
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 .
Ⅰ.尿素是一种非常重要的高氮化肥,工业上合成尿素的反应如下:
2NH3(l)+CO2(g)?H2O(l)+H2NCONH2(l)△H=-103.7kJ?mol-1
试回答下列问题:
(1)下列措施中有利于提高尿素的产率的是
A.采用高温 B.采用高压 C.寻找更高效的催化剂
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)?H2NCOONH4(氨基甲酸铵)(l)△H1
第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(l)△H2
某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第
②反应进行到10min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)=
③第二步反应的平衡常数K随温度的变化如图Ⅱ所示,则△H20
Ⅱ.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表.
工厂污染物排放浓度及允许排放标准
| 污染物 | H2SO4 | As |
| 浓度 | 28.42g/L | 1.6g?L-1 |
| 排放标准 | pH6~9 | 0.5mg?L-1 |
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
(3)若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol?L-1,c(AsO43-)最大是
(4)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式
(5)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降.
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为
考点:化学平衡的影响因素,化学反应速率的影响因素,难溶电解质的溶解平衡及沉淀转化的本质,"三废"处理与环境保护
专题:化学平衡专题,电离平衡与溶液的pH专题
分析:(1)依据化学平衡2NH3(l)+CO2(g)?H2O(l)+H2NCONH2(l)△H=-103.7kJ?mol-1,反应时气体体积减小的放热反应,结合平衡移动原理分析判断提高尿素的产率,平衡正向进行;
(2)①已知总反应的快慢由慢的一步决定,结合图象变化趋势,图象表达反应的判断,反应快慢可以依据第一步和第二步反应的曲线斜率比较大小;当氨基甲酸铵、尿素物质的量不再变化时,反应达到平衡;
②根据图象中二氧化碳在10 min时测得CO2的物质的量计算出用CO2表示的第一步反应的速率v(CO2);
③依据化学平衡常数的表达意义和计算分析判断平衡移动方向;
(3)依据Ksp越小,先生成沉淀,依据溶度积常数计算得到两种浓度;
(4)根据反应物和生成物结合元素化合价的变化配平方程式;
(5)①硫酸钙难溶于酸,所以酸性条件下能析出;
②H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀.
(2)①已知总反应的快慢由慢的一步决定,结合图象变化趋势,图象表达反应的判断,反应快慢可以依据第一步和第二步反应的曲线斜率比较大小;当氨基甲酸铵、尿素物质的量不再变化时,反应达到平衡;
②根据图象中二氧化碳在10 min时测得CO2的物质的量计算出用CO2表示的第一步反应的速率v(CO2);
③依据化学平衡常数的表达意义和计算分析判断平衡移动方向;
(3)依据Ksp越小,先生成沉淀,依据溶度积常数计算得到两种浓度;
(4)根据反应物和生成物结合元素化合价的变化配平方程式;
(5)①硫酸钙难溶于酸,所以酸性条件下能析出;
②H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀.
解答:
解:(1)A.采用高温,反应是放热反应,平衡向着逆向进行,尿素的产率降低,故A错误;
B.反应由气体参加,反应前后气体体积减小,采用高压,增大压强,反应正向进行,尿素的产率增大,故B正确;
C.寻找更高效的催化剂,催化剂可以加快反应速率,但不改变平衡,尿素的产率不变,故C错误;
故选B;
(2)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二部反应,从曲线斜率不难看出第二部反应速率慢,所以已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第二步决定,由图象变化可知当进行到55分钟时,反应达到平衡,
故答案为:2;
②反应进行到10 min时测得CO2的物质的量为0.26mol,二氧化碳的浓度变化为:c(CO2)=
=1.48mol/L,则用CO2表示的第一步反应的速率v(CO2)=
=0.148 mol/(L?min),
故答案为:0.148 mol/(L?min);
③第二步反应的平衡常数K随温度的升高增大,说明反应是吸热反应,△H2>0,
故答案为:>;
(3)若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol?L-1,依据Ksp大小可以得到,Ksp(FeAsO4 )小,反应过程中Fe3+先析出沉淀;依据Ksp(FeAsO4 )=c(Fe3+)c(AsO43-)=5.7×10-21;Fe3+的浓度均为1.0×10-4mol?L-1,计算得到 c(AsO43-)=5.7×10-17mol/L,
故答案为:5.7×10-17;
(4)三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸)同时生成Mn2+和H2O,则该反应的离子方程式为:2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O,
故答案为:2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O;
(5)①硫酸钙难溶于酸,所以酸性条件下能析出,因此pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为CaSO4,故答案为:CaSO4;
②H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀,
故答案为:H3AsO4是弱酸,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀.;
B.反应由气体参加,反应前后气体体积减小,采用高压,增大压强,反应正向进行,尿素的产率增大,故B正确;
C.寻找更高效的催化剂,催化剂可以加快反应速率,但不改变平衡,尿素的产率不变,故C错误;
故选B;
(2)①由图象可知在15分钟左右,氨气和二氧化碳反应生成氨基甲酸铵后不再变化发生的是第一步反应,氨基甲酸铵先增大再减小最后达到平衡,发生的是第二部反应,从曲线斜率不难看出第二部反应速率慢,所以已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第二步决定,由图象变化可知当进行到55分钟时,反应达到平衡,
故答案为:2;
②反应进行到10 min时测得CO2的物质的量为0.26mol,二氧化碳的浓度变化为:c(CO2)=
| 1mol-0.26mol |
| 0.5L |
| 1.48mol/L |
| 10min |
故答案为:0.148 mol/(L?min);
③第二步反应的平衡常数K随温度的升高增大,说明反应是吸热反应,△H2>0,
故答案为:>;
(3)若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol?L-1,依据Ksp大小可以得到,Ksp(FeAsO4 )小,反应过程中Fe3+先析出沉淀;依据Ksp(FeAsO4 )=c(Fe3+)c(AsO43-)=5.7×10-21;Fe3+的浓度均为1.0×10-4mol?L-1,计算得到 c(AsO43-)=5.7×10-17mol/L,
故答案为:5.7×10-17;
(4)三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸)同时生成Mn2+和H2O,则该反应的离子方程式为:2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O,
故答案为:2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O;
(5)①硫酸钙难溶于酸,所以酸性条件下能析出,因此pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为CaSO4,故答案为:CaSO4;
②H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀,
故答案为:H3AsO4是弱酸,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀.;
点评:本题考查了化学平衡的影响因素分析、化学反应速率计算等知识,溶液中浓度的换算,沉淀溶解平衡的溶度积常数计算,离子方程式的书写,沉淀的形成等,考查的知识点较多,题目难度中等,注意明确影响化学平衡的因素及化学反应速率的计算方法,试题能够提高学生的分析、理解能力及计算能力.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
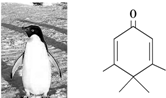 如右图所示的分子酷似企鹅,化学家将该分子以企鹅来取名为Penguinone.下列有关说法错误的是( )
如右图所示的分子酷似企鹅,化学家将该分子以企鹅来取名为Penguinone.下列有关说法错误的是( )| A、Penguinone分子式为C10H14O |
| B、Penguinone是一种芳香族化合物 |
| C、Penguinone可以使酸性高锰酸钾溶液褪色 |
| D、Penguinone能与H2发生加成反应 |
设NA为阿伏加德罗常数,下列叙述中错误的是( )
| A、在标准状况下,22.4L空气中约有NA个气体分子 |
| B、在含4mol Si-O键的石英晶体中,氧原子的数目为2NA |
| C、28g乙烯和28g丙烯中均含有6NA对共用电子对 |
| D、含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2:3 |
下列元素中,金属性最强的是( )
| A、K | B、Al | C、He | D、S |
某烷烃的结构简式为: ,下列命名正确的是( )
,下列命名正确的是( )
 ,下列命名正确的是( )
,下列命名正确的是( )| A、2,3-二甲基戊烷 |
| B、2-3-二甲基戊烷 |
| C、2-甲基-3-乙基戊烷 |
| D、2-乙基-3-甲基丁烷 |
下列说法正确的是( )
| A、NaCl和SiC晶体熔化时,克服微粒间作用力的类型相同 |
| B、24Mg32S晶体中电子总数与中子总数之比为1:1 |
| C、用乙醇或CCl4可提取碘水中的碘单质 |
| D、H2S和SiF4分子中各原子最外层都满足8电子结构 |
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.