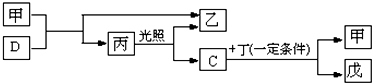
题目内容
学好《化学与技术》,对发展经济和人类的可持续发展具有重要意义.
(1)在炼铁、制玻璃、制水泥三种工业生产中,都需要的原料是 .
A.纯碱 B.石英 C.石灰石 D.黏土
(2)下列措施不能减少二氧化碳排放的是 .
A.大力发展纯电动汽车
B.关停小火电厂
C.推广使用太阳能产品
D.推广煤的气化、液化技术
(3)下列叙述错误的是 .
A.石油裂解的主要产物是乙烯
B.氨氧化法制硝酸的尾气不需净化就直接排放
C.工业上制硫酸主要分造气、催化氧化和吸收三个阶段
D.目前海水淡化的主要方法有蒸馏法、电渗析法、离子交换法等
(4)钢铁在潮湿的空气中易发生 (填“化学”或“电化学”)腐蚀.全世界每年因生锈而损失的钢铁约占钢铁产量的四分之一,请写出一种金属保护的方法 .
(1)在炼铁、制玻璃、制水泥三种工业生产中,都需要的原料是
A.纯碱 B.石英 C.石灰石 D.黏土
(2)下列措施不能减少二氧化碳排放的是
A.大力发展纯电动汽车
B.关停小火电厂
C.推广使用太阳能产品
D.推广煤的气化、液化技术
(3)下列叙述错误的是
A.石油裂解的主要产物是乙烯
B.氨氧化法制硝酸的尾气不需净化就直接排放
C.工业上制硫酸主要分造气、催化氧化和吸收三个阶段
D.目前海水淡化的主要方法有蒸馏法、电渗析法、离子交换法等
(4)钢铁在潮湿的空气中易发生
考点:常见的生活环境的污染及治理,金属的电化学腐蚀与防护
专题:元素及其化合物,化学应用
分析:(1)从碳酸钙的性质着手分析,石灰石的主要成分是碳酸钙,高温下碳酸钙和二氧化硅能发生化学反应
(2)减少二氧化碳排放,应减少含碳物质的使用;
(3)A.石油裂解可生成短链的烯烃;
B.氮氧化物污染环境;
C.工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧造气、催化氧化、吸收;
D.蒸馏法、电渗析法、离子交换法等都可淡化海水.
(4)钢铁易发生电化学腐蚀,可用刷漆、涂油、覆盖保护层、电镀、制成合金(改变金属内部结构)、牺牲阳极法、外加电流法等方法防腐.
(2)减少二氧化碳排放,应减少含碳物质的使用;
(3)A.石油裂解可生成短链的烯烃;
B.氮氧化物污染环境;
C.工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧造气、催化氧化、吸收;
D.蒸馏法、电渗析法、离子交换法等都可淡化海水.
(4)钢铁易发生电化学腐蚀,可用刷漆、涂油、覆盖保护层、电镀、制成合金(改变金属内部结构)、牺牲阳极法、外加电流法等方法防腐.
解答:
解:(1)生产玻璃的原料是纯碱、石灰石和石英,高温下,碳酸钠、碳酸钙和二氧化硅反应分别生成硅酸钠、硅酸钙;生产水泥以黏土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥,同时,石灰石还是炼铁的一种原料(造渣材料),所以在炼铁、制玻璃、制水泥三种工业生产中都用到的原料是石灰石,
故答案为:C;
(2)A.大力发展纯电动汽车,可减少化石能源的使用,减少二氧化碳的排放,故A正确;
B.关停小火电厂,可减少燃煤的使用,减少二氧化碳的排放,故B正确;
C.推广使用太阳能产品,可减少化石能源的使用,减少二氧化碳的排放,故C正确;
D.推广煤的气化、液化技术,能使煤燃烧充分,但不能减少二氧化碳的排放,故D错误.
故答案为:D;
(3)A.石油裂解可生成短链的烯烃,主要得到乙烯,故A正确;
B.氮氧化物污染环境,可导致酸雨、光化学烟雾等污染,故B错误;
C.工业制硫酸通常以黄铁矿为原料经过如下反应三步:
第一步:SO2的制取(造气).主要原料是黄铁矿和空气,在高温下煅烧,使硫元素转变成SO2气体,反应方程式为4FeS2+11O2
2Fe2O3+8SO2,设备为沸腾炉;
第二步:SO3的制取(催化氧化).从沸腾炉中出来的气体需经过净化、除尘,进入接触室在催化剂作用下SO2和O2反应生成SO3,设备为接触室;
第三步:硫酸的生成(吸收).从接触室中出来的气体进入吸收塔,为避免酸雾形成需用98.3%浓H2SO4吸收,故C正确;
D.蒸馏法、电渗析法、离子交换法等都可淡化海水,为常用方法,故D正确.
故答案为:B;
(4)钢铁易发生电化学腐蚀,可用刷漆、涂油、覆盖保护层、电镀、制成合金(改变金属内部结构)、牺牲阳极法、外加电流法等方法防腐,
故答案为:电化学;刷漆、涂油、覆盖保护层、电镀、制成合金(改变金属内部结构)、牺牲阳极法、外加电流法等.
故答案为:C;
(2)A.大力发展纯电动汽车,可减少化石能源的使用,减少二氧化碳的排放,故A正确;
B.关停小火电厂,可减少燃煤的使用,减少二氧化碳的排放,故B正确;
C.推广使用太阳能产品,可减少化石能源的使用,减少二氧化碳的排放,故C正确;
D.推广煤的气化、液化技术,能使煤燃烧充分,但不能减少二氧化碳的排放,故D错误.
故答案为:D;
(3)A.石油裂解可生成短链的烯烃,主要得到乙烯,故A正确;
B.氮氧化物污染环境,可导致酸雨、光化学烟雾等污染,故B错误;
C.工业制硫酸通常以黄铁矿为原料经过如下反应三步:
第一步:SO2的制取(造气).主要原料是黄铁矿和空气,在高温下煅烧,使硫元素转变成SO2气体,反应方程式为4FeS2+11O2
| ||
第二步:SO3的制取(催化氧化).从沸腾炉中出来的气体需经过净化、除尘,进入接触室在催化剂作用下SO2和O2反应生成SO3,设备为接触室;
第三步:硫酸的生成(吸收).从接触室中出来的气体进入吸收塔,为避免酸雾形成需用98.3%浓H2SO4吸收,故C正确;
D.蒸馏法、电渗析法、离子交换法等都可淡化海水,为常用方法,故D正确.
故答案为:B;
(4)钢铁易发生电化学腐蚀,可用刷漆、涂油、覆盖保护层、电镀、制成合金(改变金属内部结构)、牺牲阳极法、外加电流法等方法防腐,
故答案为:电化学;刷漆、涂油、覆盖保护层、电镀、制成合金(改变金属内部结构)、牺牲阳极法、外加电流法等.
点评:本题考查较为综合,涉及化学环境与污染、工业制硫酸、金属的腐蚀与防护等知识,为高频考点,侧重于化学与生活、生产、环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
在某未知溶液中检验出含有Ba2+、NO3-,且溶液的pH=1.某学生还需鉴定此溶液中是否大量存在①Al3+ ②NH4+ ③Fe2+ ④Cl- ⑤AlO2- ⑥SO42- 其实这些离子中有一部分不必再鉴定就能加以否定,你认为不必再鉴定的离子组是( )
| A、③⑤⑥ | B、④⑤⑥ |
| C、①②⑤ | D、①③④ |
桂皮酸、布洛芬和阿司匹林均为某些药物的有效成分,其结构简式如下:
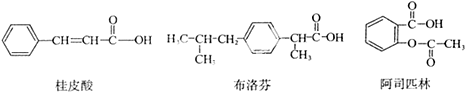
以下关于这三种有机物的说法中,不正确的是( )

以下关于这三种有机物的说法中,不正确的是( )
| A、都能与Na2CO3溶液反应产生CO2 |
| B、一定条件下,均能与乙醇发生取代反应 |
| C、只有桂皮酸可与溴的四氯化碳溶液发生加成反应 |
| D、1mol阿司匹林最多能与2mol NaOH反应 |
a、b、c、d都是短周期元素,原子半径d>c>a>b,其中a、b处在同一周期,a、c处在同一主族.c原子核内质子数等于a、b原子核内质子数之和,c原子最外层上的电子数是d原子最外层电子数的4倍.下列说法中不正确的( )
| A、a、c两元素位于元素周期表的IVA族 |
| B、d单质在b单质中燃烧生成的化合物中阴阳离子个数比为1:1 |
| C、单质c可以和d的最高价氧化物的水化物发生反应 |
| D、工业上可用单质a冶炼单质c |
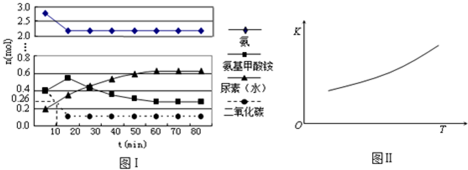
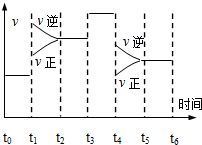 2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.
2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.