题目内容
【题目】下列过程的离子方程式书写正确的是( )
A.Cu与AgNO3溶液反应: Cu + Ag+![]() Ag + Cu2+
Ag + Cu2+
B.醋酸与氢氧化钠溶液反应: CH3COOH + OH![]() CH3COO + H2O
CH3COO + H2O
C.碳酸氢钠与硫酸反应: CO32 + 2H+![]() CO2↑ + H2O
CO2↑ + H2O
D.氢氧化铁胶体的制备:Fe2+ + 3H2O ![]() Fe(OH)3↓ + 3H+
Fe(OH)3↓ + 3H+
【答案】B
【解析】
A. Cu与AgNO3发生置换反应,生成硝酸铜和银单质,方程式为:Cu + 2AgNO3![]() 2Ag + Cu( NO3)2,离子方程式为:Cu + 2Ag+
2Ag + Cu( NO3)2,离子方程式为:Cu + 2Ag+![]() 2Ag + Cu2+,A项错误;
2Ag + Cu2+,A项错误;
B. 醋酸与氢氧化钠溶液反应,生成醋酸钠和水,反应方程式为:CH3COOH + NaOH![]() CH3COONa + H2O,离子方程式为:CH3COOH + OH
CH3COONa + H2O,离子方程式为:CH3COOH + OH![]() CH3COO + H2O,B项正确;
CH3COO + H2O,B项正确;
C. 碳酸氢钠与硫酸反应,生成硫酸钠、水和CO2,反应方程式为:NaHCO3 +H2SO4![]() 2CO2↑ + 2H2O+Na2SO4,离子方程式为:HCO3 + H+
2CO2↑ + 2H2O+Na2SO4,离子方程式为:HCO3 + H+![]() CO2↑ + H2O,C项错误;
CO2↑ + H2O,C项错误;
D. 氢氧化铁胶体的制备方程式为:FeCl3 + 3H2O ![]() Fe(OH)3(胶体)+ 3HCl,离子方程式为:Fe3+ + 3H2O
Fe(OH)3(胶体)+ 3HCl,离子方程式为:Fe3+ + 3H2O ![]() Fe(OH)3 (胶体)+ 3H+,D项错误;
Fe(OH)3 (胶体)+ 3H+,D项错误;
答案选B。

【题目】第Ⅷ族元素![]() 、
、![]() 、
、![]() 性质相似,称为铁系元素,主要用于制造合金。回答下列问题:
性质相似,称为铁系元素,主要用于制造合金。回答下列问题:
(1)基态![]() 原子核外能量最高的电子位于_______能级,同周期元素中,基态原子未成对电子数与
原子核外能量最高的电子位于_______能级,同周期元素中,基态原子未成对电子数与![]() 相同的元素名称为______________。
相同的元素名称为______________。
(2)![]() 与酚类物质的显色反应常用于其离子检验,已知
与酚类物质的显色反应常用于其离子检验,已知![]() 遇邻苯二酚(
遇邻苯二酚(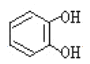 )和对苯二酚(
)和对苯二酚(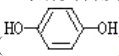 )均显绿色。邻苯二酚的熔沸点比对苯二酚_____(填“高”或“低”),原因是_________。
)均显绿色。邻苯二酚的熔沸点比对苯二酚_____(填“高”或“低”),原因是_________。
(3)有历史记载的第一个配合物是![]() (普鲁士蓝),该配合物的内界为__________。表为
(普鲁士蓝),该配合物的内界为__________。表为![]() 、
、![]() 不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,
不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,![]() 比较稳定的配离子配位数是__________(填“4”或“6”)。
比较稳定的配离子配位数是__________(填“4”或“6”)。![]() 性质活泼,易被还原,但
性质活泼,易被还原,但![]() 很稳定,可能的原因是________________。
很稳定,可能的原因是________________。
离子 | 配位数 | 晶体场稳定化能(Dq) |
| 6 | -8Dq+2p |
4 | -5.34Dq+2p | |
| 6 | -12Dq+3p |
4 | -3.56Dq+3p |
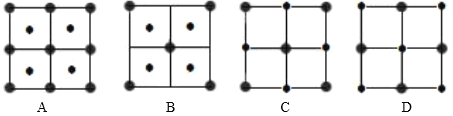
(4)![]() 晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是_______(填选项字母)。若晶胞参数为apm,阿伏加德罗常数的值为
晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是_______(填选项字母)。若晶胞参数为apm,阿伏加德罗常数的值为![]() ,晶体的密度是________
,晶体的密度是________![]() 。
。