题目内容
【题目】第Ⅷ族元素![]() 、
、![]() 、
、![]() 性质相似,称为铁系元素,主要用于制造合金。回答下列问题:
性质相似,称为铁系元素,主要用于制造合金。回答下列问题:
(1)基态![]() 原子核外能量最高的电子位于_______能级,同周期元素中,基态原子未成对电子数与
原子核外能量最高的电子位于_______能级,同周期元素中,基态原子未成对电子数与![]() 相同的元素名称为______________。
相同的元素名称为______________。
(2)![]() 与酚类物质的显色反应常用于其离子检验,已知
与酚类物质的显色反应常用于其离子检验,已知![]() 遇邻苯二酚(
遇邻苯二酚( )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚_____(填“高”或“低”),原因是_________。
)均显绿色。邻苯二酚的熔沸点比对苯二酚_____(填“高”或“低”),原因是_________。
(3)有历史记载的第一个配合物是![]() (普鲁士蓝),该配合物的内界为__________。表为
(普鲁士蓝),该配合物的内界为__________。表为![]() 、
、![]() 不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,
不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,![]() 比较稳定的配离子配位数是__________(填“4”或“6”)。
比较稳定的配离子配位数是__________(填“4”或“6”)。![]() 性质活泼,易被还原,但
性质活泼,易被还原,但![]() 很稳定,可能的原因是________________。
很稳定,可能的原因是________________。
离子 | 配位数 | 晶体场稳定化能(Dq) |
| 6 | -8Dq+2p |
4 | -5.34Dq+2p | |
| 6 | -12Dq+3p |
4 | -3.56Dq+3p |
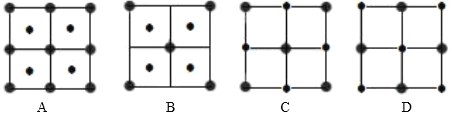
(4)![]() 晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是_______(填选项字母)。若晶胞参数为apm,阿伏加德罗常数的值为
晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是_______(填选项字母)。若晶胞参数为apm,阿伏加德罗常数的值为![]() ,晶体的密度是________
,晶体的密度是________![]() 。
。
【答案】3d 钛、锗、硒 低 邻苯二酚形成分子内氢键,比对苯二酚易形成的分子间氢键作用力小,熔沸点低 ![]() 6 形成配位键后,三价钴的氧化性减弱,性质变得稳定 CD
6 形成配位键后,三价钴的氧化性减弱,性质变得稳定 CD ![]()
【解析】
(1)![]() 为28号元素,基态
为28号元素,基态![]() 的电子排布式为[Ar]3d84s2,核外能量最高的电子位于3d能级;根据基态
的电子排布式为[Ar]3d84s2,核外能量最高的电子位于3d能级;根据基态![]() 的电子排布式为[Ar]3d84s2,其3d能级上未成对电子数为2,同周期中,未成对电子数为2的还有:钛为22号元素,基态电子排布式为:[Ar]3d24s2、锗为32号元素,基态电子排布式为:[Ar]3d104s24p2、硒为34号元素,基态电子排布式为:[Ar]3d104s24p4,故答案为:钛、锗、硒;
的电子排布式为[Ar]3d84s2,其3d能级上未成对电子数为2,同周期中,未成对电子数为2的还有:钛为22号元素,基态电子排布式为:[Ar]3d24s2、锗为32号元素,基态电子排布式为:[Ar]3d104s24p2、硒为34号元素,基态电子排布式为:[Ar]3d104s24p4,故答案为:钛、锗、硒;
(2)邻苯二酚易形成分子内氢键,对苯二酚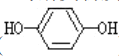 易形成的分子间氢键,后者分子间作用力较大,因此,
易形成的分子间氢键,后者分子间作用力较大,因此,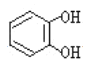 熔沸点较低;
熔沸点较低;
(3)配合物是![]() 中内界为
中内界为![]() ;由表中数据可知,配位数为6的
;由表中数据可知,配位数为6的![]() 晶体场稳定化能为-12Dq+3p,其能量降低的更多,能量越低越稳定;
晶体场稳定化能为-12Dq+3p,其能量降低的更多,能量越低越稳定;![]() 性质活泼,但
性质活泼,但![]() 很稳定,说明形成配位键后,三价钴的氧化性减弱,性质变得稳定;
很稳定,说明形成配位键后,三价钴的氧化性减弱,性质变得稳定;
(4)![]() 晶体结构中阴阳离子的配位数均为6,晶胞的俯视图应类似于NaCl晶胞,而NaCl晶胞俯视图为CD;从晶体中最小重复单元出发,1个晶胞中含Ni2+为
晶体结构中阴阳离子的配位数均为6,晶胞的俯视图应类似于NaCl晶胞,而NaCl晶胞俯视图为CD;从晶体中最小重复单元出发,1个晶胞中含Ni2+为![]() ,含O2-为
,含O2-为![]() 即根据各微粒在晶胞中位置计算出每个NiO晶胞中含4个NiO, NiO的摩尔质量75g/mol,晶体的密度除以1个晶胞的质量除以1个晶胞的体积,即为
即根据各微粒在晶胞中位置计算出每个NiO晶胞中含4个NiO, NiO的摩尔质量75g/mol,晶体的密度除以1个晶胞的质量除以1个晶胞的体积,即为![]() =
= ![]()
![]() ,故答案为:
,故答案为:![]() 。
。

【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式(或离子方程式)的类推正确的是( )
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中: Fe + Cu2+ = Cu + Fe2+ | 将Na加入到CuSO4溶液中: 2Na + Cu2+ = Cu + 2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至溶液呈中性: 2H++SO42﹣+Ba2++2OH﹣=BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应呈中性: 2H++SO42﹣+Ba++2OH﹣=BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2: Ca2++2ClO﹣+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2: Ca2++2ClO﹣+SO2+H2O=CaSO3↓+2HClO |
A.AB.BC.CD.D
【题目】氮是化肥工业和化工生产的主要原料,工业上合成氨使用的氢气主要来自合成气(CO、H2混合气体)。请回答下列问题:
(1)工业上合成氨的反应原理为N2(g)+3H2(g)![]() 2NH3(g) ΔH 。 已知:
2NH3(g) ΔH 。 已知:
化学键 | H-H | N≡N | N-H |
键能/kJ·mol-1 | 436 | 945.6 | 391 |
化学键的键能是形成或断裂1 mol 化学键放出或吸收的能量,单位为kJ/mol。上述反应的ΔH________________。
(2)联氨(又称肼,N2H4),试写出联氨的电子式_________;联氨又可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH1
N2H4(l)+O2(g)= N2(g)+2H2O(g) ΔH2
则N2(g)+2O2(g)=N2O4 (l) ΔH3=_________
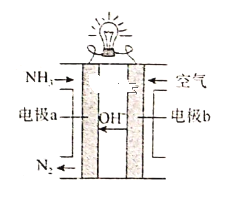
(3)以氨气代替氢气来研发氨燃料电池是当前科研的一个热点。氨燃料电池使用的电解质溶液是KOH溶液,其装置如图所示。a电极反应式为________。若该燃料电池消耗标准状况下6.72 L空气(假设空气中O2体积分数为20%),则理论上消耗NH3的质量为_______g。
(4)甲醇燃料电池在生活应用也很广泛,在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。写出该电池的负极反应式______________。