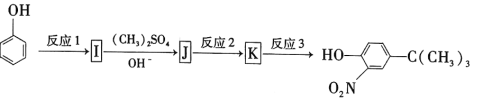
题目内容
【题目】某有机物的分子式为C4HmO,下列说法错误的是( )
A.1 mol该有机物完全燃烧时,最多消耗6 mol O2
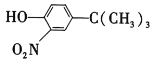
B.当m=6时,该有机物遇到FeCl3溶液发生显色反应
C.当m=8时,该有机物不一定能被新制氢氧化铜悬浊液氧化
D.当m=10时,该有机物不一定是丁醇
【答案】B
【解析】
A.m可取的最大值为10,故消耗的氧气最多为![]() ,故A正确;
,故A正确;
B.当m=6时,该有机物的分子式为C4H6O,有机物中不含酚羟基,遇氯化铁溶液不发生显色反应,故B错误;
C.当m=8时,该有机物的分子式为C4H8О,可能为醛也可能为酮,如为酮则与新制氢氧化铜悬浊液不反应,故C正确;
D.当m=10时,该有机物的分子式为C4H10O,可能为醇也可能为醚,故D正确;
故答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】A、B、C、D、E、F六种元素原子序数依次增大,前四种为短周期元素,E、F位于第四周期。已知A是自然界中含量最多的元素;B、C、D同周期,且B在同周期元素中第一电离能最小;C的第一、二、三电离能分别为738 kJ·mol1、1451 kJ·mol1、7733 kJ·mol1;D在同周期元素中(除稀有气体元素外)第一电离能最大;E元素为金属元素,常用于合成催化剂,其基态原子的价电子数为7;F元素的某种高价盐可用作城市饮用水的净水剂,比D的单质用于净水更安全环保,F基态原子的3d能级上有6个电子。
(1)试写出下列四种元素的元素符号:A_____;B_____;E_____;F_________。
(2)写出A、B两种元素组成的所有化合物的化学式:_____________。
(3)写出电解CD2的化学方程式:_____。
(4)E、F均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
元素 | E | F | |
电离能/ kJ·mol1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
E元素位于第ⅦB族,请画出基态E2+的价电子排布图:_____,F元素在周期表中的位置是_____。比较两元素的I2、I3可知,气态基态E2+再失去1个电子比气态基态F2+再失去1个电子更难,对此你的解释是:_____。
【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I: CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g) ![]() H1
H1
反应II:CO2(g)+3H2(g)![]() CH3OH(g)+ H2O(g)
CH3OH(g)+ H2O(g) ![]() H2
H2
①上述反应符合“原子经济”原则的是____________(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为______________热反应(填“吸”或“放”)。
③某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分发生反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为_______,此时的温度为_______(从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ![]() H1kJ/mol
H1kJ/mol
②2CO(g)+O2(g)=2CO2(g) ![]() H2kJ/mol
H2kJ/mol
③H2O(g)=H2O(l) ![]() H3 kJ/mol
H3 kJ/mol
则反应 CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ![]() H=________kJ/mol
H=________kJ/mol
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用如图装置模拟该法:
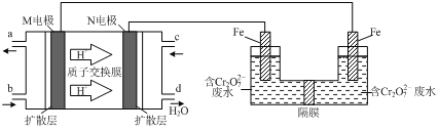
①N电极的电极反应式为____________。
②请完成电解池中Cr2O72-转化为Cr3+的离子反应方程式:
Cr2O72-+_______Fe2+ +________ [___]═ ________Cr3++_______Fe3++_________[___]