题目内容
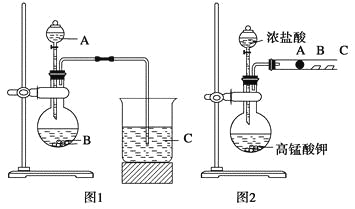
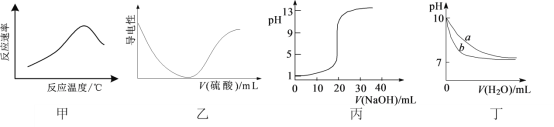
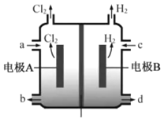
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。请根据如图所示,回答下列问题:

(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应化学方程式为__________。
(3)当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状况),丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
【答案】原电池 CH3OH+8OH--6e-=CO32-+6H2O 阳极 4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3 280 D 1.6 减小 增大
4Ag+O2↑+4HNO3 280 D 1.6 减小 增大
【解析】
(1)甲池为原电池,燃料在负极失电子发生氧化反应,在碱溶液中生成碳酸盐,甲池中通入CH3OH电极的电极反应为:CH3OH+8OH--6e-=CO32-+6H2O;
(2)乙池是电解池,A为阳极,B为阴极,电池中是电解硝酸银溶液生成银,硝酸和氧气,电池反应为4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3;
4Ag+O2↑+4HNO3;
(3)当乙池中B极质量增加5.4g Ag,其物质的量=![]() =0.05mol,根据电子守恒计算4Ag~O2~4e-,甲池中理论上消耗O2的体积=
=0.05mol,根据电子守恒计算4Ag~O2~4e-,甲池中理论上消耗O2的体积=![]() =0.28L=280mL;丙为电解池,C为阳极,D为阴极,电解氯化铜溶液,铜离子在阴极得到电子析出铜,结合电子守恒计算2Ag~Cu~2e-,析出铜质量=
=0.28L=280mL;丙为电解池,C为阳极,D为阴极,电解氯化铜溶液,铜离子在阴极得到电子析出铜,结合电子守恒计算2Ag~Cu~2e-,析出铜质量=![]() =1.6g;
=1.6g;
(4)甲中发生的反应为甲醇与氧气、氢氧化钾的反应,反应消耗氢氧根离子,则pH减小,丙中电极不变,将其溶液换成NaCl溶液,则丙中电解NaCl溶液生成氢氧化钠,所以溶液pH增大。

【题目】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生如下反应:2NO(g)+O2(g)![]() 2NO2(g),下列各项能说明反应达到平衡状态的是_____________。
2NO2(g),下列各项能说明反应达到平衡状态的是_____________。
A.体系压强保持不变
B.混合气体颜色保持不变
C.NO和O2的物质的量之比保持不变
D.每消耗1 molO2同时生成2 molNO
(2)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),达平衡后测得各组分浓度:
CH3OH(g),达平衡后测得各组分浓度:
物质 | CO | H2 | CH3OH |
浓度(mol/L) | 0.9 | 1.0 | 0.6 |
回答下列问题:
①混合气体的平均相对分子质量=_________________。
②平衡常数K=__________________。
③若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是__________。
④若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正______v逆(填“>”、“<”或“=”)。