题目内容
【题目】核磁共振氢谱是研究有机物结构的有力手段之一。
(1)分子式均为C3H6O2的两种混合物,在核磁共振氢谱上观察到氢原子的峰有两种情况,第一种情况中峰面积比是1:1,第二种情况中峰面积之比为3:2:1,由此推断该混合物的组成可能是__(写出一种情况即可)。
(2)有一种有机物的分子式为C7H8O,苯环上有1个羟基,请写出该有机物可能的结构简式__,核磁共振氢谱上观察到氢原子的峰面积比为__(对应上一空所填物质)。
【答案】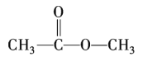 、
、
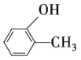 、
、![]() 、
、![]() 1:1:1:1:1:3、1:1:1:1:1:3、1:2:2:3
1:1:1:1:1:3、1:1:1:1:1:3、1:2:2:3
【解析】
在核磁共振氢谱上观察到氢原子峰面积之比等于不同环境的氢原子个数之比,如峰面积之比为1:1,说明有2种氢原子,且个数比为1:1;峰面积之比为3:2:1,说明有3种氢原子,且个数比为3:2:1,据此分析。
(1)分子式均为C3H6O2的两种混合物,峰面积之比为1:1,说明有2种氢原子,且个数比为1:1,结构简式为CH3COOCH3;峰面积之比为3:2:1,说明有3种氢原子,且个数比为3:2:1,结构简式为CH3CH2COOH、HCOOCH2CH3或CH3COCH2OH;
(2)有机物的分子式为C7H8O,已知苯环上有一个羟基,则推出还有一个甲基;根据苯环上有两个取代基的位置关系,可确定甲基和羟基的位置关系为相邻、相间、相对,则可能的结构简式为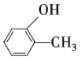 、
、![]() 、
、![]() 。
。 的氢原子的峰面积比为1:1:1:1:1:3;
的氢原子的峰面积比为1:1:1:1:1:3;![]() 的氢原子的峰面积比为1:1:1:1:1:3;
的氢原子的峰面积比为1:1:1:1:1:3;![]() 的氢原子的峰面积比为1:2:2:3。
的氢原子的峰面积比为1:2:2:3。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目