题目内容
9.元素A的原子最外层有6个电子,元素B的原子最外层有3个电子,则A与B形成的化合物可能的化学式是( )| A. | B2A3 | B. | B2A | C. | BA2 | D. | BA |
分析 元素A的原子最外层有6个电子,则最高化合价为+6价,最低化合价为-2价,元素B的原子最外层有3个电子,反应中易失去3个电子,化合价为+3价,根据化合物化合价代数和为0解答.
解答 解:元素A的原子最外层有6个电子,则最高化合价为+6价,最低化合价为-2价,元素B的原子最外层有3个电子,反应中易失去3个电子,化合价为+3价,A、B发生化合反应时,生成化合物中A为-2价,B为+3价,对应的化合物应为B2A3,故选A.
点评 本题考查原子结构与元素的性质,题目难度不大,注意元素化合价与最外层电子数的关系,注意化合物化合价代数和为0的原则.

练习册系列答案
相关题目
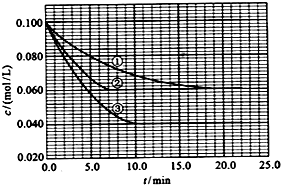
19. 已知CO和H2在一定条件下合成甲醇的反应为CO(g)+2H2(g)?CH3OH(g),现在容积固定且相等的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度进行反应,测得相关数据的关系如图所示.下列说法正确的是( )
已知CO和H2在一定条件下合成甲醇的反应为CO(g)+2H2(g)?CH3OH(g),现在容积固定且相等的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度进行反应,测得相关数据的关系如图所示.下列说法正确的是( )
 已知CO和H2在一定条件下合成甲醇的反应为CO(g)+2H2(g)?CH3OH(g),现在容积固定且相等的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度进行反应,测得相关数据的关系如图所示.下列说法正确的是( )
已知CO和H2在一定条件下合成甲醇的反应为CO(g)+2H2(g)?CH3OH(g),现在容积固定且相等的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度进行反应,测得相关数据的关系如图所示.下列说法正确的是( )| A. | a容器中,0~5min反应速率v(H2)=0.08mol•L-1•min-1 | |
| B. | 反应进行到5min时,b容器中v正=v速 | |
| C. | 其他条件不变时,减压可将b中的状态转变成c中的状态 | |
| D. | 达到平衡时a、b、c容器中的转化率为b>a>c |
20.下列化学肥料中属于复合肥的是( )
| A. | KNO3 | B. | CO(NH2)2 | C. | Ca3(PO4)2 | D. | K2SO4 |
4.下列说法中正确的是( )
| A. | 完全由非金属组成的化合物不一定是共价化合物 | |
| B. | 构成分子晶体的粒子一定含有共价键 | |
| C. | 分子晶体的熔点一定比金属晶体的熔点低 | |
| D. | 含有金属离子的晶体一定是离子晶体 |
14.分别向含有下列离子的溶液中通入足量NO2气体,数目不会减少的是( )
| A. | SO${\;}_{3}^{2-}$ | B. | CH3COO- | C. | Fe2+ | D. | Al3+ |
1.a、b、c、d均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )
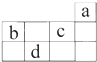

| A. | a原子的最外电子层上有8个电子 | |
| B. | c的最高价氧化物对应水化物为强酸 | |
| C. | d的原子半径比c的原子半径大 | |
| D. | b的气态氢化物比c的气态氢化物稳定 |
18.已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,根据化学方程式:N2+3H2$?_{高温高压}^{催化剂}$2NH3,1mol N2与足量H2反应放出的热量为92.4kJ•mol-1,那么N≡N键的键能是( )
| A. | 431kJ•mol-1 | B. | 945.6kJ•mol-1 | C. | 649kJ•mol-1 | D. | 896kJ•mol-1 |
 稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.