题目内容
【题目】标况下,一容积不变的密闭容器里充满硫化氢和氧气的混合气体,点燃恰好完全反应后,恢复至原状态,压强变为原来的![]() ,计算原混合气体的硫化氢和氧气的体积比________。
,计算原混合气体的硫化氢和氧气的体积比________。
【答案】4∶5
【解析】
硫化氢燃烧可以发生反应:①2H2S+O2![]() 2S+2H2O,②2H2S+3O2
2S+2H2O,②2H2S+3O2![]() 2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的
2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的![]() ,根据方程式对应关系可以求得答案。
,根据方程式对应关系可以求得答案。
硫化氢燃烧可以发生反应:①2H2S+O2![]() 2S+2H2O,②2H2S+3O2
2S+2H2O,②2H2S+3O2![]() 2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的
2SO2+2H2O,反应前后都在标况下,恢复至原状态,若只发生①,反应后压强为0;若只发生反应②,反应后压强变为原来的![]() 。由题目信息得压强变为原来的
。由题目信息得压强变为原来的![]() ,则反应①、②都发生。又根据相同条件下压强之比等于气体物质的量之比,假设反应后气体物质的量为1mol,即反应后二氧化硫的物质的量为1mol,则反应前混合气体总物质的量为3 mol,则根据反应:
,则反应①、②都发生。又根据相同条件下压强之比等于气体物质的量之比,假设反应后气体物质的量为1mol,即反应后二氧化硫的物质的量为1mol,则反应前混合气体总物质的量为3 mol,则根据反应:
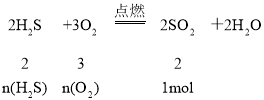
n(H2S)=1mol,n(O2)=1.5mol,消耗的H2S和O2分别为1mol和1.5mol,故硫化氢燃烧生成硫与水的反应中,n(H2S)+n(O2)=3mol-1mol-1.5mol=0.5 mol。由反应:2H2S+O2![]() 2S↓+2H2O,可知n(H2S)=0.5 mol×
2S↓+2H2O,可知n(H2S)=0.5 mol×![]() =
=![]() mol,n(O2)=0.5 mol×
mol,n(O2)=0.5 mol×![]() =
=![]() mol。原混合气体的硫化氢和氧气的体积比等于其物质的量之比,为(1 mol+
mol。原混合气体的硫化氢和氧气的体积比等于其物质的量之比,为(1 mol+![]() mol)∶(1.5 mol+
mol)∶(1.5 mol+![]() mol)=4∶5。
mol)=4∶5。

【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 室温下,向苯酚钠溶液中通足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
B | 加热乙醇与浓硫酸的混合溶液,将产生的气体通入少量酸性KMnO4溶液,溶液紫红色褪去 | 有乙烯生成 |
C | 向5 mL 0.1 mol·L1 KI溶液中加入1 mL 0.1 mol·L1 FeCl3溶液,充分反应后,萃取分液,向水层中滴加KSCN溶液,溶液呈血红色 | I-与Fe3+的反应有一定限度 |
D | 向NaHCO3溶液中滴加紫色石蕊试液,溶液变蓝 | Kw<Ka1(H2CO3)×Ka2(H2CO3) |
A.AB.BC.CD.D
【题目】在800℃时,2L密闭容器内发生反应:2NO(g)+O2(g)2NO2(g),反应体系中,一氧化氮的物质的量随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)如图表示NO2的物质的量浓度变化的曲线是________。
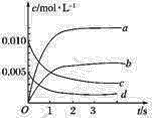
(2)用O2表示从0~2 s内该反应的平均速率v=__________。
(3)能说明该反应已达到平衡状态的是________。
A.v(NO2)=2v(O2)
B.容器内压强保持不变
C.容器内气体质量不变
D.容器内密度保持不变