题目内容
【题目】双缩脲反应可以用于测定蛋白质的含量。双缩脲反应的原理可表示如下:
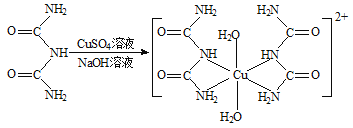
双缩脲 紫红色配离子
(1)Cu2+的基态核外电子排布式为_______。
(2)与H2O互为等电子体的一种阳离子为_______(填化学式)。
(3)双缩脲分子中氮原子轨道的杂化类型是_______;1 mol双缩脲分子中含有σ键的数目为_______。
(4)该紫红色配离子中的配位原子为_______。
(5)Cu3Au的晶胞如下图所示,Cu3Au晶体中每个铜原子周围距离最近的铜原子数目为_______。

【答案】[Ar]3d9或1s22s22p63s23p63d9 H2F+ sp3 11 NA或11×6.02×1023 N、O 8
【解析】
根据构造原理写出铜原子的核外电子排布式,再写出铜离子的核外电子排布式。根据同族替换或等量代换寻找等电子体。根据氮原子的成键类型,判断杂化方式。根据单键是σ键,双键中一个是σ键一个是π键,找到直接和中心原子相连的的配位体的原子是配位原子。根据Cu和Au的位置,找到每个铜原子周围距离最近的铜原子数目。
(1)铜是29号元素,铜原子的核外电子排布式为:[Ar]3d104s1或1s22s22p63s23p63d104s1,Cu2+的基态核外电子排布式为[Ar]3d9或1s22s22p63s23p63d9;
(2) H2O的价电子数为8个,原子个数为3个,与H2O互为等电子体的一种阳离子为H2F+;
(3)双缩脲分子中氮原子成三个共价键,含有一个孤电子对,杂化类型是sp3杂化,根据双缩脲分子的结构,单键是σ键,双键中一个是σ键一个是π键,1 mol双缩脲分子中含有σ键的物质的量为11mol,数目为11 NA或11×6.02×1023;
(4)该紫红色配离子中与铜离子直接相连的原子是N、O,配位原子为N、O;
(5)Cu3Au的晶胞中,Cu 位于面心,Au位于顶点,Cu3Au晶体中每个铜原子周围距离最近的铜原子数目为8,位于此晶胞侧面的四个铜原子和位于上面的晶胞的侧面,共8个。

 期末1卷素质教育评估卷系列答案
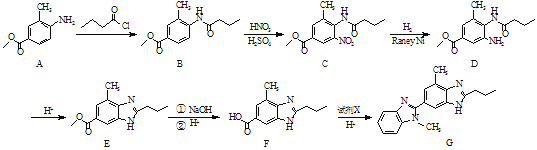
期末1卷素质教育评估卷系列答案【题目】某实验小组设计实验,利用酸性KMnO4溶液与H2C2O4溶液反应,测定溶液紫色消失所需时间的方法,研究浓度对反应速率的影响。供选择的实验药品有:0.01mol·L-1酸性KMnO4溶液、0.1mol·L-1酸性KMnO4溶液、0.1mol·L-1H2C2O4溶液、0.2mol·L-1H2C2O4溶液。
(1)H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为_______________。
(2)请完成以下实验设计表。
实验 | 酸性KMnO4溶液 | H2C2O4溶液 | 褪色时间/s | ||
c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
甲 | 0.01 | 4 | 0.1 | 2 | t1 |
乙 | a | 4 | b | 2 | t2 |
①表中a=________、b=________;
②甲组实验KMnO4的平均反应速率是:____________(用含t1的式子表示)。
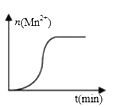
(3)测得某次实验(恒温)时,溶液中Mn2+物质的量与时间关系如图。请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因:___________________。