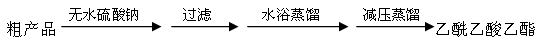题目内容
难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下平衡:
K2SO4·MgSO4·2CaSO4·2H2O(s)
 2Ca2++2K++Mg2++4
2Ca2++2K++Mg2++4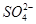 +2H2O
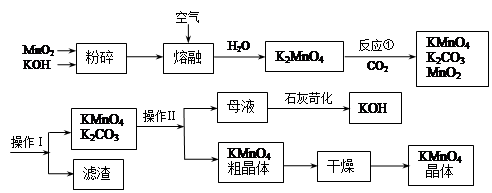
+2H2O为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:
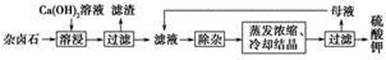
(1)滤渣主要成分有________和________以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:_________________________________________________。
(3)“除杂”环节中,先加入________溶液,经搅拌等操作后,过滤,再加入________溶液调滤液pH至中性。
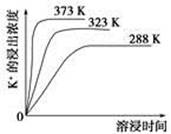
(4)不同温度下,K+的浸出浓度与溶浸时间的关系如图。由图可得,随着温度升高,
①________________________________________________________,
②________________________________________________________。
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+
 ?
? CaCO3(s)+
CaCO3(s)+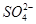
已知298 K时,Ksp(CaCO3)=2.80×10-9,
Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K(计算结果保留三位有效数字)。
(1)Mg(OH)2 CaSO4
(2)加入Ca(OH)2溶液,Mg2+与OH-结合生成Mg(OH)2沉淀,Mg2+浓度减小,平衡正向移动,K+增多
(3)K2CO3 H2SO4
(4)①溶浸平衡向右移动 ②K+的溶浸速率增大
(5)CaSO4(s)+
 CaCO3(s)+
CaCO3(s)+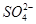 的平衡常数
的平衡常数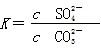 ,据Ksp(CaSO4).Ksp(CaCO3)可知:
,据Ksp(CaSO4).Ksp(CaCO3)可知: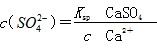 ,则有
,则有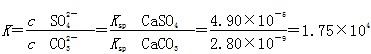 。
。
(2)加入Ca(OH)2溶液,Mg2+与OH-结合生成Mg(OH)2沉淀,Mg2+浓度减小,平衡正向移动,K+增多
(3)K2CO3 H2SO4
(4)①溶浸平衡向右移动 ②K+的溶浸速率增大
(5)CaSO4(s)+

 CaCO3(s)+
CaCO3(s)+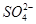 的平衡常数
的平衡常数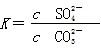 ,据Ksp(CaSO4).Ksp(CaCO3)可知:
,据Ksp(CaSO4).Ksp(CaCO3)可知: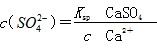 ,则有
,则有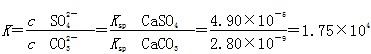 。
。解题时,要依据制备K2SO4的工艺流程,结合物质的分离与提纯的原则进行分析。
(1)杂卤石中加入Ca(OH)2溶液,Mg2+与OH-结合生成Mg(OH)2沉淀,CaSO4微溶于水,过滤后,滤渣中含有Mg(OH)2.CaSO4及未溶解的杂卤石。
(2)加入Ca(OH)2溶液,Mg2+与OH-结合生成Mg(OH)2沉淀,使c(Mg2+)减小,杂卤石的溶解平衡正向移动,同时c(Ca2+)与c(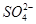 )均增大,从而析出CaSO4沉淀,K+留在滤液中。
)均增大,从而析出CaSO4沉淀,K+留在滤液中。
(3)滤液中含有Ca2+.OH-,可先加入过量K2CO3溶液,除去Ca2+,过滤后,再加入稀H2SO4调节溶液的pH至中性。
(4)①溶浸平衡向右移动;②K+的溶浸速率增大。
(1)杂卤石中加入Ca(OH)2溶液,Mg2+与OH-结合生成Mg(OH)2沉淀,CaSO4微溶于水,过滤后,滤渣中含有Mg(OH)2.CaSO4及未溶解的杂卤石。
(2)加入Ca(OH)2溶液,Mg2+与OH-结合生成Mg(OH)2沉淀,使c(Mg2+)减小,杂卤石的溶解平衡正向移动,同时c(Ca2+)与c(
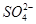 )均增大,从而析出CaSO4沉淀,K+留在滤液中。
)均增大,从而析出CaSO4沉淀,K+留在滤液中。(3)滤液中含有Ca2+.OH-,可先加入过量K2CO3溶液,除去Ca2+,过滤后,再加入稀H2SO4调节溶液的pH至中性。
(4)①溶浸平衡向右移动;②K+的溶浸速率增大。

练习册系列答案
相关题目

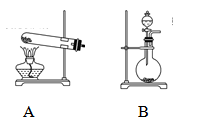
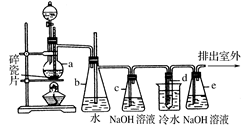
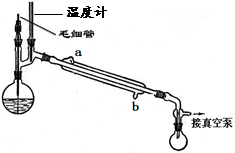
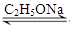 CH3COCH2COOC2H5+C2H5OH。反应中催化剂乙醇钠是由金属钠和残留在乙酸乙酯中的微量乙醇作用生成的,而一旦反应开始,生成的乙醇又会继续和钠反应生成乙醇钠。乙酰乙酸乙酯制备的流程如下:
CH3COCH2COOC2H5+C2H5OH。反应中催化剂乙醇钠是由金属钠和残留在乙酸乙酯中的微量乙醇作用生成的,而一旦反应开始,生成的乙醇又会继续和钠反应生成乙醇钠。乙酰乙酸乙酯制备的流程如下: