题目内容
【题目】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照以下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2%H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(1)实验①和②的目的是______________________。
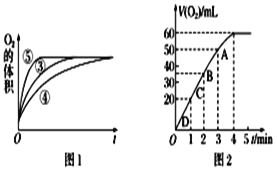
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图1。分析图1能够得出的实验结论是(Ⅰ)____________。(Ⅱ)_____________。
(3)加入0.1 g MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图2所示。反应速率逐渐变化的原因是________________。
【答案】 探究H2O2溶液浓度的变化对分解速率的影响 FeCl3对H2O2的分解有催化作用 碱性条件比酸性条件催化效果好 H2O2的浓度逐渐减小
【解析】(1)实验①和②的浓度不同,则该实验的目的为探究浓度对化学反应速率的影响;反应物浓度越大反应速率越快;因此,本题正确答案是:探究浓度对反应速率的影响;
(2)实验③④⑤中都加了1 mL 0.1 mol·L-1FeCl3溶液做催化剂,加快了化学反应速度,所以FeCl3对H2O2的分解有催化作用;由图可以知道,⑤的反应速率最大,④的反应速率最小,结合实验方案可以知道,碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率,
因此答案是: I FeCl3对H2O2的分解有催化作用,II碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率。
(3) 随时间的推移,反应物过氧化氢的浓度逐渐减小,浓度越小反应速率越慢, 应速率逐渐变化的原因是D、C、B、A四点H2O2的浓度逐渐减小,化学反应速率也逐减慢,因此本题正确答案是: H2O2的浓度逐渐减小