题目内容
11.若NA表示阿伏加德罗常数,下列有关叙述正确的是( )| A. | 标准状况下,44.8L苯中分子数为2NA | |
| B. | 1mol水中含氢离子数为NA | |
| C. | 5.6g铁与足量稀硫酸完全反应失去电子数为0.3NA | |
| D. | 16gCH4与18gNH4+ 所含电子数均为10NA |
分析 A、标况下,苯为液体;
B、水是弱电解质,不能完全电离;
C、求出铁的物质的量,然后根据铁与稀硫酸反应变为+2价来分析;
D、求出16gCH4与18gNH4+ 的物质的量,然后根据CH4与NH4+ 均为10电子微粒来分析.
解答 解:A、标况下,苯为液体,不能用气体摩尔体积来计算其物质的量,故A错误;
B、水是弱电解质,不能完全电离,故1mol水中含有的氢离子小于1mol,即小于NA个,故B错误;
C、5.6g铁的物质的量为0.1mol,而铁与稀硫酸反应变为+2价,故0.1mol铁失去0.2mol电子,故C错误;
D、16gCH4与18gNH4+ 的物质的量均为1mol,而CH4与NH4+ 均为10电子微粒,故1molCH4与NH4+均含10mol电子,个数为10NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的运用以及物质的状态和结构是解题关键,难度不大.

练习册系列答案
相关题目
1.如图所示能够组成原电池,并且产生明显的电流的是( )
| A. |  | B. |  | C. |  | D. |  |
2.有机物M的结构简式为: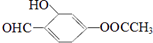 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | M的分子式为:C9H8O4 | |
| B. | M与乙酸苯乙酯互为同系物 | |
| C. | M可发生水解反应、加成反应、氧化反应 | |
| D. | 1mol M可与3mol NaOH和2mol Br2发生反应 |
6.下列装置中能将电能转化为化学能的是( )
| A. |  | B. |  | C. | 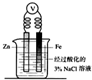 | D. | 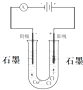 |
3.下列有关物质应用的说法正确的是( )
| A. | 玻璃容器可长期盛放各种酸 | B. | P2O5可用于干燥Cl2和NH3 | ||
| C. | Si和SiO2都用于制造光导纤维 | D. | Na2S可除去污水中的Cu2+ |
20.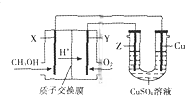 用甲醇燃料电池电解硫酸铜溶液的装置如图所示,其中X、Y、Z均为惰性电极.甲醇在燃料电池的X电极上产生质子:CH3OH+H2O-e-→CO2+H+(未配平)经质子交换膜到达Y电极;电解一段时间后,在U型管的溶液汇总加入0.1molCu2(OH)2CO3,反应后恰好恢复为电解前的硫酸铜溶液.则下列有关说法正确的是( )
用甲醇燃料电池电解硫酸铜溶液的装置如图所示,其中X、Y、Z均为惰性电极.甲醇在燃料电池的X电极上产生质子:CH3OH+H2O-e-→CO2+H+(未配平)经质子交换膜到达Y电极;电解一段时间后,在U型管的溶液汇总加入0.1molCu2(OH)2CO3,反应后恰好恢复为电解前的硫酸铜溶液.则下列有关说法正确的是( )
 用甲醇燃料电池电解硫酸铜溶液的装置如图所示,其中X、Y、Z均为惰性电极.甲醇在燃料电池的X电极上产生质子:CH3OH+H2O-e-→CO2+H+(未配平)经质子交换膜到达Y电极;电解一段时间后,在U型管的溶液汇总加入0.1molCu2(OH)2CO3,反应后恰好恢复为电解前的硫酸铜溶液.则下列有关说法正确的是( )
用甲醇燃料电池电解硫酸铜溶液的装置如图所示,其中X、Y、Z均为惰性电极.甲醇在燃料电池的X电极上产生质子:CH3OH+H2O-e-→CO2+H+(未配平)经质子交换膜到达Y电极;电解一段时间后,在U型管的溶液汇总加入0.1molCu2(OH)2CO3,反应后恰好恢复为电解前的硫酸铜溶液.则下列有关说法正确的是( )| A. | Y为燃料电池的正极,其电极反应为:O2+2H2O+4e-═4OH- | |
| B. | 此电解过程中,Z电极上的反应始终为:2H2O-4e-═4H++O2↑ | |
| C. | 电解过程中中铜电极不会被溶解,其原理为牺牲阳极的阴极保护法 | |
| D. | 电子沿着X→Cu→Z→Y路径移动,每个电极均通过0.6mole- |
1.化学与资源、环境、生活关系密切,下列说法不正确的是( )
| A. | 将镁块与钢铁输水管相连,可防止钢铁腐蚀 | |
| B. | 推广使用新能源,可以减少二氧化碳等温室气体的排放 | |
| C. | 焊锡中加铅的目的是降低熔点 | |
| D. | 石油是混合物,其分馏产品汽油为纯净物 |
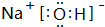 、
、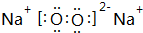 .
.