题目内容
11.下列实验中,所选装置不合理的是( )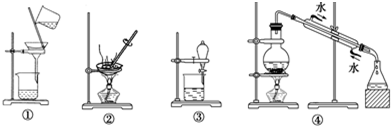
| A. | 分离Na2CO3溶液和CH3COOC2H5,选③ | |
| B. | 用CCl4提取碘水中的碘,选③和④ | |
| C. | 除去氯化钠中的少量硝酸钾固体,选②和① | |
| D. | 模拟血液透析,选① |
分析 图①过滤是分离固体与液体混合物;
图②是蒸发结晶或降为结晶,分离溶解度随着温度变化不同的溶质;
图③为分液是分离互不相溶的两种液体;
图④是蒸馏分离的是相互溶解的沸点不同的两种液体.
解答 A.碳酸钠与乙酸乙酯互不相溶,用分液法分离,故A正确;
B.用CCl4提取碘水中的碘,通过分液得到碘的四氯化碳溶液,然后通过蒸馏分离二者,故B正确;
C.氯化钠随着温度变化溶解度变化不大,硝酸钾溶解度随着温度变化很明显,可以通过降温结晶分离,故C正确;
D.血液属于胶体,能够通过滤纸,应选择半透膜进行渗析,故D错误;
故选:D.
点评 本题考查物质的分离、提纯的方法,题目难度不大,注意把握物质的性质的异同,结合不同分离方法使用的原理分离.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
1.下列说法正确的是( )
| A. | 常温pH=11的烧碱溶液与pH=3的稀醋酸等体积混合后,滴入石蕊试液呈红色 | |
| B. | T℃时,pH=6的纯水中,含10-8NA个OH-(NA表示阿伏加德罗常数) | |
| C. | 将NaAlO2、FeCl3、Al2(SO4)3的水溶液分别在蒸发皿中加热、蒸干并灼烧,都能得原溶质 | |
| D. | 常温下由水电离的c(H+)=1×10-13mol/L的溶液里,能大量存在NH4+、Fe2+、NO3- |
2.以下化学反应的离子方程式书写正确的是( )
| A. | H2CO3电离:H2CO3?2H++CO32- | |
| B. | 将少量金属钠放入冷水中:Na+2H2O═Na++2OH-+H2↑ | |
| C. | C12溶解于水:H2O+Cl2?2H++ClO-+Cl- | |
| D. | 向CuSO4溶液中通入H2S:Cu2++H2S═CuS↓+2H+ |
19.下列说法正确的是( )
| A. | 淀粉与纤维素互为同分异构体 | |
| B. | 乙烯能和溴水、酸性高锰酸钾溶液发生加成反应使之褪色 | |
| C. | 汽油、柴油和植物油都是碳氢化合物,完全燃烧只生成CO2和H2O | |
| D. | 淀粉、油脂、蛋白质都能水解,但水解产物不同 |
16.下列表示对应化学反应的离子式方程式正确的是( )
| A. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O+CO32- | |
| B. | 漂白粉溶液中通入过量CO2气体:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | |
| C. | 向NH4Al(SO4)2溶液中逐渐滴入加入Ba(OH)2溶液恰好使SO42-反应完全: 2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O | |
| D. | FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
3. 向Ba(OH)2和NaOH的混合溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如图所示,下列说法不正确的是( )
向Ba(OH)2和NaOH的混合溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如图所示,下列说法不正确的是( )
 向Ba(OH)2和NaOH的混合溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如图所示,下列说法不正确的是( )
向Ba(OH)2和NaOH的混合溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如图所示,下列说法不正确的是( )| A. | a点之前的反应化学方程式为:CO2+Ba(OH)2=BaCO3↓+H2O | |
| B. | a~b之间的反应离子方程式为:CO2+2OH-=CO${\;}_{3}^{2-}$+H2O | |
| C. | c点CO2的体积应为15.0L | |
| D. | 原混合溶液中Ba(OH)2和NaOH的浓度之比为1:1 |
20.在溶液中能大量共存的微粒组是( )
| A. | K+、CH3COOH、CO32-、NO3- | B. | Fe3+、Na+、SCN-、Cl- | ||
| C. | Ba2+、Na+、OH-、HCO3- | D. | H+、K+、Fe3+、NO3- |
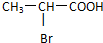 ;
;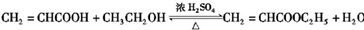 ,该反应的反应类型为酯化反应(或取代反应);
,该反应的反应类型为酯化反应(或取代反应);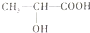 ,试写出C与金属Na反应的化学方程式为:
,试写出C与金属Na反应的化学方程式为: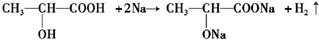 .
. ③白磷 ④氯气 ⑤2,2-二甲基丁烷 ⑥氯水 ⑦
③白磷 ④氯气 ⑤2,2-二甲基丁烷 ⑥氯水 ⑦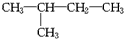 ⑧CH3(CH2)3CH3 ⑨${\;}_{17}^{35}$Cl ⑩红磷⑪${\;}_{17}^{37}$Cl⑫
⑧CH3(CH2)3CH3 ⑨${\;}_{17}^{35}$Cl ⑩红磷⑪${\;}_{17}^{37}$Cl⑫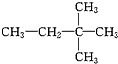 ⑬CH2=CH2⑭CH2=CH-CH=CH2
⑬CH2=CH2⑭CH2=CH-CH=CH2 ;取代反应.
;取代反应. ;取代反应.
;取代反应.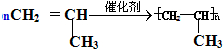 ;加聚反应.
;加聚反应.