��Ŀ����
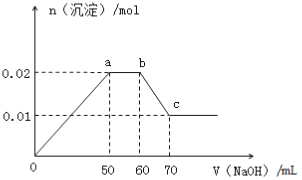
����Ŀ��ij��ɫ��Һ�к���Mg2+��Al3+��Fe3+��Cu2+��NH4+��Na+�е�һ�ֻ��֣�ȡ100mL����Һ�������в��ϵμ�NaOH��Һ�������ij�������NaOH����仯�Ĺ�ϵ��ͼ��ʾ����������������ȷ����
A. ����Һ��һ������Fe3+��Cu2+
B. ����Һ��һ������Mg2+��Al3+��NH4+�����������ʵ���Ũ��֮��Ϊ1:1:2
C. ����NaOH��Һ���ʵ���Ũ��Ϊ1mol/L
D. a�㵽b�㣬NH4++OH- =NH3��H2O
���𰸡�B
�����������������ij��ɫ��Һ�к���Mg2+��Al3+��Fe3+��Cu2+��NH4+��Na+�е�һ�ֻ�������һ��û��Fe3+��Cu2+��ȡ100mL����Һ�������в��ϵμ�NaOH��Һ�������ij�������NaOH����仯�Ĺ�ϵ��ͼ��ʾ����ͼ��֪��0~50���������ӵ��������50~60����������˵��һ����NH4+��60~70�����ܽ���һ�룬˵����������Al(OH)3��Mg(OH)2��������Һ��һ����Mg2+��Al3+��NH4+�����ɳ����ı仯��֪n(Mg2+)=n(Al3+)=0.01mol����0~50mL����Һ�з��������ӷ�ӦΪAl3++3OH-=Al(OH)3����Mg2++2OH-=Mg(OH)2����50~60mL�� a�㵽b��������Һ�з��������ӷ�ӦΪNH4++OH-=NH3H2O�������ӷ���ʽ�������������ĵ�����������Һ�������֪��NH4+�����ʵ�����Mg2+��Al3+��ͬ������NH4++OH-=NH3H2O�������c(NaOH)= ![]() =1mol/L������������B����ȷ������ѡB.
=1mol/L������������B����ȷ������ѡB.

 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�