题目内容
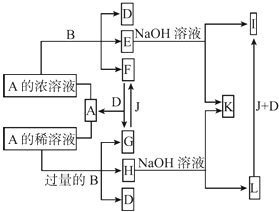
【题目】A~M为中学化学的常见物质,它们之间的转化关系如图所示,部分生成物和反应条件省略.已知C、D是由元素X、Y、Z中的两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色气体且不能燃烧,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.请回答下列问题: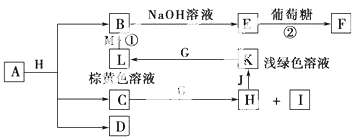
(1)写出A的化学式: .
(2)比较Y与Z的原子半径大小:>(填元素符号).
(3)检验L溶液中金属阳离子的方法是 .
(4)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体.请写出该反应的化学方程式: .
【答案】
(1)CuCO3或Cu(OH)2(CO3)2
(2)C;O
(3)取少量L溶液于试管中,滴加KSCN溶液,如溶液呈血红色,证明含有Fe3+
(4)3Cu2O+14HNO3(稀)=6Cu(NO3)2+2NO↑+7H2O
【解析】解:已知C、D是由元素X、Y、Z中的两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,则X为H元素;Y、Z原子最外层电子数之和为10,D为无色气体且不能燃烧,D为CO2 , Y为C元素、Z为O元素;L为棕黄色溶液,则L中含有Fe3+ , K为浅绿色溶液,则K中含有Fe2+ , G为黄绿色单质气体,则G为Cl2 , 故L为FeCl3 , K为FeCl2 , 反应①常用于制作印刷电路板,则金属M为Cu,B为CuCl2 , E为Fe(OH)2 , F为Cu2O,由氯气与C反应生成H,H与金属J反应得到FeCl2 , 则H为HCl,I有漂白作用,所以I为HClO,C为水,则A为CuCO3或Cu(OH)2(CO3)2 . (1)A的化学式:CuCO3或Cu(OH)2(CO3)2 , 所以答案是:CuCO3或Cu(OH)2(CO3)2;(2)Y为C元素,Z为O元素,原子半径C>O,所以答案是:C;O;(3)检验L(FeCl3)溶液中金属阳离子的方法是:取少量L溶液于试管中,滴加KSCN溶液,如溶液呈血红色,证明含有Fe3+ , 所以答案是:取少量L溶液于试管中,滴加KSCN溶液,如溶液呈血红色,证明含有Fe3+ , (4)F(Cu2O)溶于稀硝酸,溶液变成蓝色,放出无色气体,反应生成硝酸铜、NO与水,反应的化学方程式:3Cu2O+14HNO3(稀)=6Cu(NO3)2+2NO↑+7H2O,
所以答案是:3Cu2O+14HNO3(稀)=6Cu(NO3)2+2NO↑+7H2O.

【题目】某探究小组利用丙酮的溴代反应(CH3COCH3+Br2 ![]() CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
实验序号 | 初始浓度c/molL﹣1 | 溴颜色消失所需的时间t/s | ||
CH3COCH3 | HCl | Br2 | ||
① | 0.80 | 0.20 | 0.0010 | 290 |
② | 1.60 | 0.20 | 0.0010 | 145 |
③ | 0.80 | 0.40 | 0.0010 | 145 |
④ | 0.80 | 0.20 | 0.0020 | 580 |
分析实验数据所得出的结论不正确的是( )
A.增大c(CH3COCH3),v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大
D.增大c(Br2),v(Br2)增大