��Ŀ����
����Ŀ��̽����Ƭ��Na2CO3��Һ�ķ�Ӧ��
| | |
���������� | ��Ƭ�������ϸС���� | ���ְ�ɫ���ǣ������������ݣ�������ΪH2��CO2�� |
����˵������ȷ����
A. Na2CO3��Һ�д���ˮ��ƽ�⣺CO32- + H2O HCO3- + OH-
B. �ԱȢ�˵��Na2CO3��Һ���ƻ�������ı���Ĥ
C. �Ʋ���ְ�ɫ���ǵ�ԭ��AlO2- + HCO3- + H2O = Al(OH)3��+ CO32-
D. ���Ⱥ�H2�ݳ���CO32- ˮ��ƽ���ƶ������Ӱ�����෴��
���𰸡�D
��������
A. ��Һ��̼�����ˮ�⣬���ˮ������������ӣ�����̼�������A����ȷ�����������⣻
B��ʵ���͢�û�����ݣ�������ѧAl���Ժ���ˮ��Ӧ�����Ǵ�ʵ����û�����ݣ�˵��������Ĥ�ı�����ʵ�����ȴ�����ݣ�˵������Ĥ���ƻ���B����ȷ�����������⣻
C��Na2CO3��Һ�ʼ��ԣ���Ƭ�ڼ�����Һ����OH����Ӧ������ƫ�������2Al��2OH����2H2O=2AlO2����3H2����AlO2����HCO3-��Ӧ������������������C����ȷ�����������⣻
D��CO32����ˮ�������ȵģ����ȿ��Դٽ�ˮ�⡣H2������ԭ����Al��CO32��ˮ�����ɵ�OH����Ӧ����H2��H2�ݳ���������Al��OH���ķ�Ӧ��OH�����٣��Ӷ��ٽ�̼���ˮ�⣬���Ⱥ�H2�ݳ���CO32- ˮ��ƽ���ƶ������Ӱ������ͬ�ģ�D����������⣻
�����ѡD��

����Ŀ��Bodensteins�о���ӦH2(g)��I2(g)![]() 2HI(g)���¶�ΪTʱ�������������Ϊ1 L���ܱ������н���ʵ�飬������������е⻯������ʵ�������w (HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
2HI(g)���¶�ΪTʱ�������������Ϊ1 L���ܱ������н���ʵ�飬������������е⻯������ʵ�������w (HI)�뷴Ӧʱ��t�Ĺ�ϵ���±���
������� | ��ʼ���� | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
I | 0.5 mol I2��0.5 mol H2 | w (HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
II | x mol HI | w (HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
�о�����������Ӧ�У�v����ka��w(H2)��w(I2)��v����kb��w2(HI)������ka��kbΪ����������˵����ȷ���ǣ�
A. �¶�ΪTʱ���÷�Ӧ![]()
B. ����I����ǰ20 min��ƽ������v(HI)=0.0125 mol��L��1��min��1
C. ����ʼʱ������I�м������ʵ�����Ϊ0.1 mol��H2��I2��HI����Ӧ�������
D. ���������д���ka��= ka����kb��= kb������x��ֵ����Ϊ�κ�ֵ
����Ŀ���о���ѧ��Ӧʱ����Ҫ�������ʱ仯�������仯����Ҫ��ע��Ӧ�Ŀ������ȡ��ش��������⣺
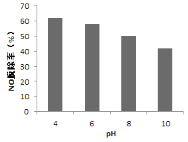
(1)NH3��ԭNO����Ҫ�����������������䷴Ӧ������������ϵ����ͼ��ʾ��

����ͼ����Ϊ�ı��˷�Ӧ��������Ӧ�Ļ��b___________(���������������)a��
��������Ӧ���Ȼ�ѧ����ʽ�ɱ�ʾΪ��Ӧ�����������H��___________(��E1�� E2�Ĵ���ʽ��ʾ)
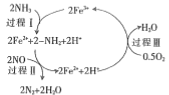
���о����֣�һ�������µ�������Ӧ���̿�����ͼ��ʾ������������ԭ��Ӧ�����ʵ����ã�NOΪ��____�������ܷ�Ӧ�Ļ�ѧ����ʽΪ��___________��
(2)һ���¶��£�����ͬ���ʵ�����H2O(g)��CO�ֱ�ͨ���ݻ�Ϊ1L�ĺ����ܱ������У����з�ӦH2O(g)+CO(g)��CO2(g)+H2(g)���õ������ʾ���������ݣ�
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
H2O(g) | CO(g) | CO(g) | H2(g) | |||
1 | 650 | 2.0 | 4.0 | 3.0 | 1.0 | 5 |
2 | 900 | 1.0 | 2.0 | 1.8 | 0.2 | 4 |
3 | 900 | a | b | c | d | t |
��ʵ��2��4min
��650��ʱ�����ڴ������г���2.0molH2O(g)��1.0molCO(g)��1.0molCO2(g)��xmolH2(g)��Ҫʹ��Ӧ�ڿ�ʼʱ��������Ӧ������У���xӦ�����������___________��
����a=2.0��b=1.0����ƽ��ʱʵ��2��H2O(g)��ʵ��3��CO(g)��ת����(��)�Ĺ�ϵΪ��(H2O)___________(�������������=��)��(CO)��