题目内容
【题目】下列热化学方程式书写正确的是( )
A.2SO2+O2![]() 2SO3 △H=-196.6kJ/mol
2SO3 △H=-196.6kJ/mol
B.C(s)+O2(g)=CO2(g) △H=+393.5kJ/mol
C.在500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
D.2.00gC2H2气体完全燃烧生成液态水和二氧化碳气体,放出99.6kJ的热量,该反应的热化学方程式为:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2589.6kJ/moL
【答案】D
【解析】
试题分析:A、反应热与物质的状态有关,不同状态的反应热不同,因此热化学反应方程式必须写明状态,故错误;B、所有燃烧都是放热反应,△H<0,故错误;C、此反应是可逆反应,不知道消耗N2或H2,生成NH3的物质的量,故错误;D、消耗2mol乙炔伴随的热效应是26×2×99.6/2kJ=2589.6kJ,故正确。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】研究含氮化合物对能源、环保和生产具有重要的意义。请回答下列问题:
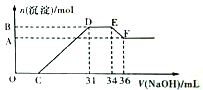
(1)在2 L密闭容器内, 800 ℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①如图所示A点处v正___(填“>”、“<”或“=”,下同)v逆,A点处v正___B点处v正。
②如图所示的曲线,其中表示NO2的变化的曲线是________(填a、b、c、d等字母)。用O2表示2 s内该反应的速率v=________。
(2)已知化学反应N2+3H2![]() 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,
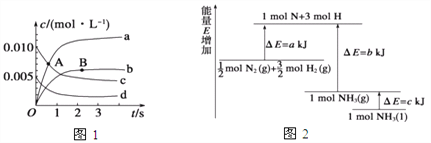
则,1 mol N和3 mol H生成1 mol NH3(g)是______能量的过程(填“吸收”或“释放”),由![]() mol N2(g)和
mol N2(g)和![]() mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。
mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。