题目内容
【题目】[化学——选修2:化学与技术]
高锰酸钾(![]() )是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为MnO2)为原料生产高锰酸钾的工艺路线如下:
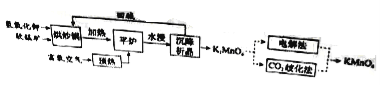
回答下列问题:
(1)原料软锰矿与氢氧化钾按1∶1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用是 。
(2)“平炉”中发生的化学方程式为 。
(3)“平炉”中需要加压,其目的是 。
(4)将K2MnO4转化为KMnO4的生产有两种工艺。
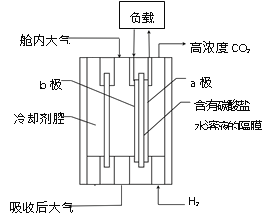
①“![]() 歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成K2MnO4,MnO2和 (写化学式)。
歧化法”是传统工艺,即在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成K2MnO4,MnO2和 (写化学式)。
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为
,阴极逸出的气体是 。
③“电解法”和“![]() 歧化法”中,K2MnO4的理论利用率之比为 。
歧化法”中,K2MnO4的理论利用率之比为 。
(5)高锰酸钾纯度的测定:称取1.0800 g样品,溶解后定容于100 mL容量瓶中,摇匀。取浓度为0.2000 mol·L1的H2C2O4标准溶液20.00 mL,加入稀硫酸酸化,用KMnO4溶液平行滴定三次,平均消耗的体积为24.48 mL,该样品的纯度为
(列出计算式即可,已知2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O)。
【答案】(1)扩大接触面积,加快化学反应速率;
(2)2MnO2+O2+4KOH![]() 2K2MnO4+2H2O;
2K2MnO4+2H2O;
(3)增大反应物的浓度,可使化学反应速率加快,同时使反应物的转化率增大;
(4) ① K2CO3;②MnO42--e-=MnO4-;③3:2;
(5)95.62%。
【解析】
试题(1) MnO2的状态是固体,对于有固体参加的化学反应,可通过增大其反应接触面积的方法提高反应速率,故要将其粉碎成细小的颗粒;(2) 根据流程图可知,在“平炉”中MnO2、KOH、O2在加热时反应产生K2MnO4,结合质量守恒定律可知,另外一种物质是H2O,则发生的化学方程式为2MnO2+O2+4KOH![]() 2K2MnO4+2H2O ;(3)由于上述反应中氧气是气体,在“平炉”中加压,就可以使反应物氧气的浓度增大,根据外界条件对化学反应速率的影响,增大反应物的浓度,可以使化学反应速率加快;任何反应都具有一定的可逆性,增大压强,可以使化学平衡向气体体积减小的正反应方向移动,故可以提高原料的转化率; (4) ①在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成KMnO4,MnO2,根据质量守恒定律可知,另外一种生成物是K2CO3,根据氧化还原反应中的电子守恒及反应的原子守恒,可得该反应的化学方程式是:3K2MnO4+ 2CO2= 2KMnO4+MnO2+K2CO3;②“电解法”为现代工艺,即电解K2MnO4水溶液,在电解槽中阳极,MnO42-失去电子,发生氧化反应,产生MnO4-。电极反应式是:MnO42--e-=MnO4-;在阴极,水电离产生的H+获得电子变为氢气逸出,电极反应式是:2H2O+2e-=H2↑+2OH-。所以阴极逸出的气体是H2;总反应方程式是:2K2MnO4+2H2O
2K2MnO4+2H2O ;(3)由于上述反应中氧气是气体,在“平炉”中加压,就可以使反应物氧气的浓度增大,根据外界条件对化学反应速率的影响,增大反应物的浓度,可以使化学反应速率加快;任何反应都具有一定的可逆性,增大压强,可以使化学平衡向气体体积减小的正反应方向移动,故可以提高原料的转化率; (4) ①在K2MnO4溶液中通入CO2气体,使体系呈中性或弱碱性,K2MnO4发生歧化反应,反应中生成KMnO4,MnO2,根据质量守恒定律可知,另外一种生成物是K2CO3,根据氧化还原反应中的电子守恒及反应的原子守恒,可得该反应的化学方程式是:3K2MnO4+ 2CO2= 2KMnO4+MnO2+K2CO3;②“电解法”为现代工艺,即电解K2MnO4水溶液,在电解槽中阳极,MnO42-失去电子,发生氧化反应,产生MnO4-。电极反应式是:MnO42--e-=MnO4-;在阴极,水电离产生的H+获得电子变为氢气逸出,电极反应式是:2H2O+2e-=H2↑+2OH-。所以阴极逸出的气体是H2;总反应方程式是:2K2MnO4+2H2O![]() 2KMnO4+2H2↑+2KOH;③根据“电解法”方程式2K2MnO4+ 2H2O
2KMnO4+2H2↑+2KOH;③根据“电解法”方程式2K2MnO4+ 2H2O![]() 2KMnO4+2H2↑+2KOH 可知K2MnO4的理论利用率是100%;而在“CO2歧化法” 3K2MnO4+2CO2 = 2KMnO4+MnO2+K2CO3中,K2MnO4的理论利用率是2/3,所以二者的理论利用率之比为3:2;(5)根据离子方程式2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O可知KMnO4与草酸反应的关系式是:2 KMnO4~5H2C2O4。配制的溶液的浓度为:
2KMnO4+2H2↑+2KOH 可知K2MnO4的理论利用率是100%;而在“CO2歧化法” 3K2MnO4+2CO2 = 2KMnO4+MnO2+K2CO3中,K2MnO4的理论利用率是2/3,所以二者的理论利用率之比为3:2;(5)根据离子方程式2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O可知KMnO4与草酸反应的关系式是:2 KMnO4~5H2C2O4。配制的溶液的浓度为:![]() 。则1.0800g样品中含KMnO4的物质的量为:n=
。则1.0800g样品中含KMnO4的物质的量为:n=![]() KMnO4的质量为:m=" 0.006536mol" × 158g/mol =1.03269g。故其纯度为:
KMnO4的质量为:m=" 0.006536mol" × 158g/mol =1.03269g。故其纯度为:![]() ×100%=95.62%。
×100%=95.62%。

 阅读快车系列答案
阅读快车系列答案【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将SO2气体通入Ba(NO3)2溶液 | 有白色沉淀 | SO2中混有SO3 |
B | 向NaAlO2溶液中持续通入气体Y | 先出现白色沉淀,最终沉淀又溶解 | Y可能是CO2气体 |
C | AgCl悬浊液中滴入少量Na2S溶液 | 沉淀变黑色 | Ksp(Ag2S)>Ksp(AgCl) |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在平衡: I3- |
A. A B. B C. C D. D
【题目】Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物,羟基自由基的产生与溶液pH大小有关。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
(实验过程)

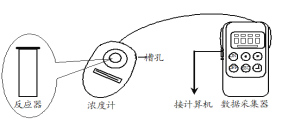
用图所示装置进行如下表所示的实验,控制p-CP的初始浓度相同,其余实验条件见下表,设计如下对比实验,最终测量的是p-CP浓度的改变量。
(实验数据)
实验编号 | H2O2溶液 | Fe2+溶液 | 蒸馏水 | pH | 温度 | ||
c/(10-3mol·L-1) | V/mL | c/(10-3mol·L-1) | V/mL | V/mL | T/K | ||
① | 6.0 | 1.5 | 0.30 | 3.5 | 10 | 3 | 298 |
② | 6.0 | 1.5 | 0.30 | 3.5 | 10 | 3 | 313 |
③ | 6.0 | 3.5 | 0.30 | 3.5 | x | 3 | 298 |
④ | 6.0 | 1.5 | 0.30 | 4.5 | 9 | 3 | 298 |
⑤ | 6.0 | 1.5 | 0.30 | 3.5 | 10 | 10 | 298 |
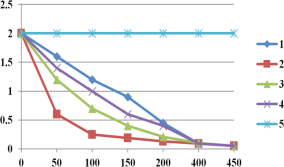
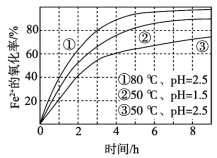
图2实验测得p-CP的浓度随时间的变化
(分析与解释)
(1)实验③中,x=________。
(2)实验①、⑤的目的是________。
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高是反而导致降解反应速率减少,从Fenton法所用试剂H2O2性质的角度分析原因_____(请用化学用语解答)。
(4)通过实验⑤可以得出结论是是pH等于10时,降解反应趋于停止,推测可能的原因:__。