题目内容
【题目】如图所示是部分短周期元素原子半径与原子序数的关系,则下列说法正确的是( )

A.M在周期表中的位置为:第二周期,IVA族
B.Y和Z两元素的离子半径相比,后者较大
C.M、N两种元素的气态氢化物的稳定性相比,后者较强
D.Y元素和X元素可以形成Y2X2型化合物,阴、阳离子物质的量之比为1:1
【答案】C
【解析】
根据图示部分短周期元素原子半径与原子序数的关系,前7种元素位于第二周期,后7种元素位于第三周期,结合原子半径大小可知,X为O元素,Y为Na元素,Z为Al,M为Si,N为Cl元素,据此解答。
根据分析可知,X为O元素,Y为Na元素,Z为Al,M为Si,N为Cl元素,
A.Si的原子序数为14,位于周期表中第三周期,第IVA族,故A错误;
B.Y离子为Na+,Z离子为Al3+,两者有相同的电子层结构,核电荷数越小,半径越大,故Na+半径大于Al3+,故B错误;
C.M为Si,N为Cl元素,同周期从左到右,气态氢化物的稳定性逐渐增强,故HCl的稳定性比SiH4强,故C正确;
D.X为O元素,Y为Na元素,Na元素和O元素形成的Na2O2中,阴离子为过氧根离子,则阴、阳离子物质的量之比为1:2,故D错误;
答案选C。

 培优好卷单元加期末卷系列答案
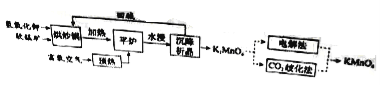
培优好卷单元加期末卷系列答案【题目】连二亚硫酸钠(Na2S2O4)是印刷行业重要的还原剂,易溶于水,难溶于乙醇;高铁酸钾(K2FeO4)是一种绿色环保型饮用水处理剂。某课题小组拟以硫铁矿(主要成分是FeS2)为主要原料制备连二亚硫酸钠和高铁酸钾,其简易工艺流程如下(部分步骤和条件略去):
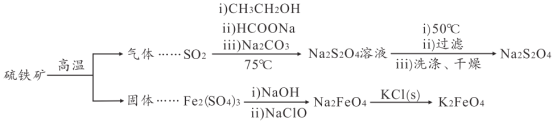
(1)FeS2中含有S22-离子,其电子式为_____。“气体”的主要成分是O2、SO2和N2,参考表中的数据,简述工业上用物理方法分离提纯二氧化硫的实验方案:_____
熔点/℃ | 沸点/℃ | 密度/gL-1(标准状况) | |
O2 | -218 | -183 | 1.429 |
SO2 | -76 | -10 | 2.9 |
N2 | -210 | -196 | 1.25 |
(2)SO2→Na2S2O4步骤中氧化剂与还原剂的物质的量之比为_____。制得的Na2S2O4溶液冷却至50℃,过滤,用_____洗涤,干燥,制得Na2S2O4。
(3)Na2FeO4与KC1发生复分解反应制备K2FeO4,说明相同温度下K2FeO4的溶解度_____(填“ > ”、“ < ”或=”) Na2FeO4的溶解度。
(4)溶液中的Na2S2O4易被空气中的氧气氧化生成NaHSO3,反应的离子方程式为_____
(5)在制备Na2FeO4时,现象是先生成红褐色沉淀,随后转化成绿色溶液,生成了 Na2FeO4。
①写出红褐色沉淀转化为Na2FeO4的化学方程式:_____。
②为探究Na2FeO4和Cl2的氧化性相对强弱,取少量上述绿色溶液于试管中,滴加适量浓盐酸,产生能使湿润的KI淀粉试纸变蓝色的气体,不能说明Na2FeO4的氧化性比Cl2的氧化性强,理由是_____。
【题目】研究化学反应的能量变化和速率变化是研究化学反应的重要角度。
(1)化学反应中能量变化的主要原因是旧的化学键断裂会_____能量;新的化学键形成会_____能量。(填“放出”或“吸收”)
(2)用铝热法可冶炼铁,其反应为:Fe2O3+2Al![]() 2Fe+Al2O3,属于放热反应,反应物的总能量______(填“>”、“=”或“<”)生成物的总能量。在该反应中,若消耗了1molAl,则理论上可炼制Fe的物质的量为_____mol。
2Fe+Al2O3,属于放热反应,反应物的总能量______(填“>”、“=”或“<”)生成物的总能量。在该反应中,若消耗了1molAl,则理论上可炼制Fe的物质的量为_____mol。
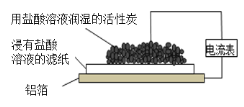
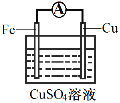
(3)为探究反应过程中的能量变化,某小组同学用如图装置进行实验。
|
|
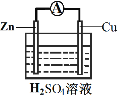
装置Ⅰ | 装置Ⅱ |
①装置Ⅰ中,Fe与CuSO4溶液反应的离子方程式是_____。
②装置Ⅱ中,正极的电极反应式为______。
③关于装置Ⅱ,下列叙述正确的是______(填字母)。
a.H+在Cu表面被还原,产生气泡
b.电流从Zn片经导线流向Cu片
c.电子从Zn片经导线流向Cu片
d.Zn和Cu的都是电极材料,也都参与电极反应
(4)某兴趣小组将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是_____。
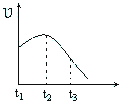
A.从t1→t2的原因是镁与酸的反应是放热反应,体系温度升高
B.从t1→t2的原因水蒸发,致使酸的浓度升高
C.从t2→t3的原因是随着反应的进行镁条的质量下降
D.从t2→t3的原因是随着反应的进行,H+的浓度逐渐下降