题目内容
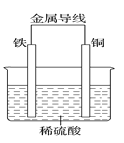
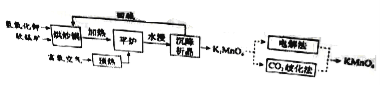
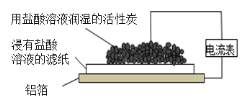
【题目】下图是在载人航天器舱内利用氢氧燃料电池进行二氧化碳浓缩富集的装置。下列说法正确的是

A. a极为电池的正极
B. b极的电极反应:2CO2 + O2 + 4e- === 2CO32-
C. 该装置工作时电能转化成了化学能
D. CO32- 向b极移动
【答案】B
【解析】
氢氧燃料电池中通入氢气的为负极,通入空气的为正极,据此分析解答。
A.氢氧燃料电池中通入氢气的为负极,因此a是负极,b是正极,故A错误;
B.b是正极,正极上氧气得电子和二氧化碳反应生成碳酸根离子,电极反应式为2CO2 + O2 + 4e- = 2CO32-,故B正确;
C.该装置为原电池,工作时化学能转化成了电能,故C错误;
D.在原电池中,阴离子向负极移动,因此CO32- 向a极移动,故D错误;
答案选B。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】某化学实验小组用酸性KMnO4溶液和草酸(H2C2O4)溶液反应,研究外界条件反应速率的影响,实验操作及现象如下:
编号 | 实验操作 | 实验现象 |
I | 向一支试管中先加入1 mL 0.01 mol/L酸性 KMnO4溶液,再加入1滴3 mol/L硫酸和9滴蒸馏水,最后加入1 mL 0.1 mol/L草酸溶液 | 前10 min内溶液紫色无明显变化,后颜色逐渐变浅, 30 min后几乎变为无色 |
II | 向另一支试管中先加入1 mL 0.01 mol/L酸性 KMnO4溶液,再加入10滴3 mol/L硫酸,最后加入1 mL 0.1 mol/L草酸溶液 | 80 s内溶液紫色无明显变化,后颜色迅速变浅,约150 s后几乎变为无色 |
(1)补全高锰酸钾与草酸反应的离子方程式:5H2C2O4 + 2MnO4- + 6H+ === 2Mn2+ + ______ +______
(2)由实验I、II可得出的结论是______。
(3)关于实验II中80 s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的Mn2+对反应有催化作用。利用提供的试剂设计实验III,验证猜想。
提供的试剂:0.01 mol/L酸性 KMnO4溶液,0.1 mol/L草酸溶液,3 mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水
① 补全实验III的操作:向试管中先加入1 mL 0.01 mol/L酸性 KMnO4溶液,______,最后加入1 mL 0.1 mol/L草酸溶液。
② 若猜想成立,应观察到的实验现象是______。
(4)该小组拟采用如下图所示的实验方案继续探究外界条件对反应速率的影响。
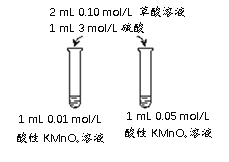
① 他们拟研究的影响因素是______。
② 你认为他们的实验方案______(填“合理”或“不合理”),理由是______。
【题目】实验小组制备高铁酸钾![]() 并探究其性质。
并探究其性质。
资料:![]() 为紫色固体,微溶于
为紫色固体,微溶于![]() 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生![]() ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1)制备![]() (夹持装置略)
(夹持装置略)
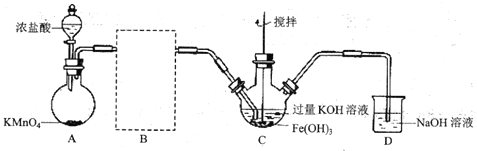
①A为氯气发生装置。A中反应的离子方程式为_________(锰被还原为![]() )。
)。
②请在B方框内将除杂装置补充完整,并标明所用试剂__________。
③![]() 中得到紫色固体和溶液。
中得到紫色固体和溶液。![]() 中主要反应的化学方程式为___________。
中主要反应的化学方程式为___________。
(2)探究![]() 的性质
的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有![]() 。为证明是否
。为证明是否![]() 氧化了
氧化了![]() 而产生
而产生![]() ,设计以下方案:
,设计以下方案:
方案Ⅰ | 取少量a,滴加 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将 |
由方案Ⅰ中溶液变红可知a中含有的离子为____,但该离子的产生不能判断一定是![]() 将
将![]() 氧化,该离子还可能由_______产生(用离子方程式表示)。
氧化,该离子还可能由_______产生(用离子方程式表示)。
②根据![]() 的制备实验得出:氧化性
的制备实验得出:氧化性___________
![]() (填“>”或“<”),而方案Ⅱ实验表明,
(填“>”或“<”),而方案Ⅱ实验表明,![]() 和
和![]() 的氧化性强弱关系相反,原因是________________。
的氧化性强弱关系相反,原因是________________。
③资料表明,酸性溶液中的氧化性![]() ,验证实验如下:将溶液
,验证实验如下:将溶液![]() 滴入
滴入![]() 和足量
和足量![]() 的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性![]() 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:_______________。
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:_______________。