题目内容
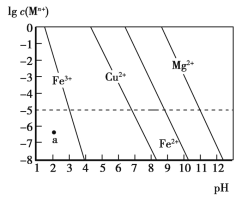
【题目】常温下,几种难溶金属氢氧化物分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图所示。下列说法正确的是
A.a点代表Fe(OH)3的饱和溶液
B.Ksp[Cu(OH)2]<Ksp[Fe(OH)2]
C.向0.1 mol·L-1Cu2+、Mg2+、Fe2+混合溶液中,逐滴滴加稀NaOH溶液,Mg2+最先沉淀
D.在pH=7的溶液中,Cu2+、Mg2+、Fe2+能大量共存
【答案】B
【解析】
A.a点c(Fe3+)远小于相同pH的饱和溶液中c(Fe3+),溶液中大都以Fe3+形式存在,所以a点表示Fe3+没有沉淀,故A错误;
B.金属的Ksp=c(Mn+)cn(OH-),Cu2+在pH=7左右完全沉淀,Fe2+在pH=9左右才完全沉淀,所以Ksp[Cu(OH)2]<Ksp[Fe(OH)2],故B正确;
C.根据图表可知,Cu2+、Mg2+、Fe2+三种离子,镁离子完全沉淀对应的pH=11左右,是三个粒子中最大的,Ksp[Mg(OH)2]最大,即镁离子最难沉淀,Cu2+在pH=7左右完全沉淀,是三个粒子中最小的,所以Cu2+最先沉淀,故C错误;
D.Cu2+在pH=7左右完全沉淀,所以在pH=7时,Cu2+主要以Cu(OH)2形式存在,故D错误。
故选B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目