题目内容
【题目】短周期主族元素W、X、Y、Z、R 原子序数依次增大。由W、X、Y、R组成的一种化合物a在加热时完全分解为三种产物,其中一种产物b是能使品红溶液褪色的气体,另一种产物c是能使湿润的红色石蕊试纸变蓝的气体。金属单质Z在空气中燃烧生成的化合物可与水发生反应生成气体。下列说法正确的是
A. 简单离子的半径: X < Z < R
B. X的简单氢化物比Y的稳定
C. a、b、c中均含有极性共价健,且 a属于电解质,b和c都属于非电解质
D. W、X、Y、R四种元素形成的化合物一定会促进水的电离
【答案】C
【解析】分析:由W、X、Y、R组成的一种化合物a在加热时完全分解为三种产物,其中一种产物b是能使品红溶液褪色的气体,另一种产物c是能使湿润的红色石蕊试纸变蓝的气体,b为SO2,C为NH3,化合物a中含有S、O、N、H四种元素,a可能为(NH4)2SO3或NH4HSO3,W、X、Y、R的原子序数依次增大,W为H元素,X为N元素,Y为O元素,R为S元素;金属单质Z在空气燃烧生成的化合物可与水反应生成气体,Z的原子序数介于O和S之间,Z为Na元素。
详解:由W、X、Y、R组成的一种化合物a在加热时完全分解为三种产物,其中一种产物b是能使品红溶液褪色的气体,另一种产物c是能使湿润的红色石蕊试纸变蓝的气体,b为SO2,C为NH3,化合物a中含有S、O、N、H四种元素,a可能为(NH4)2SO3或NH4HSO3,W、X、Y、R的原子序数依次增大,W为H元素,X为N元素,Y为O元素,R为S元素;金属单质Z在空气燃烧生成的化合物可与水反应生成气体,Z的原子序数介于O和S之间,Z为Na元素。A项,根据“层多径大,序大径小”,简单离子半径:Z![]() X
X![]() R,A项错误;B项,非金属性:N(X)
R,A项错误;B项,非金属性:N(X)![]() O(Y),X的简单氢化物不如Y的稳定,B项错误;C项,a中含离子键和极性共价键,b和c中只含极性共价键,a属于电解质,b和c都属于非电解质,C项正确;D项,W、X、Y、R四种元素形成的化合物有(NH4)2SO3、、NH4HSO3、(NH4)2SO4、NH4HSO4等,(NH4)2SO3、(NH4)2SO4发生水解促进水的电离,NH4HSO4完全电离出H+抑制水的电离,D项错误;答案选C。
O(Y),X的简单氢化物不如Y的稳定,B项错误;C项,a中含离子键和极性共价键,b和c中只含极性共价键,a属于电解质,b和c都属于非电解质,C项正确;D项,W、X、Y、R四种元素形成的化合物有(NH4)2SO3、、NH4HSO3、(NH4)2SO4、NH4HSO4等,(NH4)2SO3、(NH4)2SO4发生水解促进水的电离,NH4HSO4完全电离出H+抑制水的电离,D项错误;答案选C。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
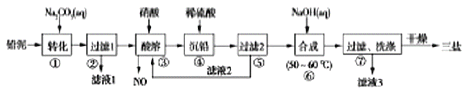
能考试全能100分系列答案【题目】工业从废铅酸蓄电池的渣泥(主要成分为PbSO4、PbO2)回收铅。RSR 工艺的主要流程如下:
![]()
(1)铅酸蓄电池放电时总反应为:
Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(l)
正极反应:PbO2(s) + SO42-(aq) + 4H+(aq) + 2e- = PbSO4(s) + 2H2O(l)
负极反应:________。
(2)向渣泥中加入Na2CO3溶液将PbSO4转化为更难溶的PbCO3。
①用化学平衡移动原理解释其原因:________。
②工业上常用NaHCO3溶液代替Na2CO3溶液,将PbSO4转化为PbCO3。PbSO4与NaHCO3溶液或Na2CO3溶液不同物质的量比时,PbSO4的转化率见下表。
Ⅰ | n(PbSO4)∶ n(NaHCO3) | 1∶1.5 | 1∶2 | 1∶3 |
PbSO4转化率/% | 95.5 | 96.9 | 97.8 | |
Ⅱ | n(PbSO4)∶ n(Na2CO3) | 1∶1.5 | 1∶2 | 1∶3 |
PbSO4转化率/% | 98 | 98 | 98 |
依据上表数据,物质的量比相同时,Ⅱ中PbSO4的转化率比Ⅰ中的略大,原因是________。
③上述反应除生成PbCO3外,还可能生成碱式碳酸铅[2PbCO3·Pb(OH)2],二者受热都易分解生成PbO。通过实验确定产物中含有2PbCO3·Pb(OH)2,则该实验操作及现象是________;通过定量实验确定产物中2PbCO3·Pb(OH)2的含量,则需测定的数据是________。
(3)渣泥中加入Na2SO3溶液,利用其性质是________。
(4)H2SiF4溶液溶解PbCO3的化学方程式是________。
【题目】下列实验操作正确且能达到相应目的的是
选项 | 实验目的 | 实验操作 |
A | 称取2.0gNaOH固体 | 先在托盘上各放1张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
B | 配制稀硫酸 | 先将浓硫酸加入烧杯,后倒入蒸馏水 |
C | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
D | 检验溶液中是否有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
A. A B. B C. C D. D