题目内容
6.在密闭容器里,通入x molH2和y mol I2(g),发生如下反应:H2(g)+I2(g)?2HI(g).改变下列条件,反应速率将如何变化?(填“增大”“减小”或“不变”)(1)升高温度增大,
(2)充入更多的H2增大,
(3)扩大容器的体积减小,
(4)容器容积不变,通入氖气不变.
分析 增大浓度、增大压强、使用催化剂,反应速率加快,扩大体积,压强减小,速率减小,恒容容器中加入惰气反应速率不变,以此解答该题.
解答 解:(1)升高温度,反应速率增大,故答案为:增大;
(2)再充入H2,反应物浓度增大,化学反应速率增大,故答案为:增大;
(3)将容器容积扩大,相当于减小压强,则反应速率减小,故答案为:减小;
(4)容器容积不变,通入氖气,反应体系中各物质的浓度不变,则反应速率不变,故答案为:不变.
点评 本题考查影响化学反应速率的因素,为高频考点,侧重于学生的分析能力的考查,题目较简单,明确常见的影响因素即可解答.

练习册系列答案
相关题目
16.下列物质性质与应用对应关系不正确的是( )
| A. | 汽油与水互不相溶,可用裂化汽油萃取溴水中的溴 | |
| B. | 明矾能水解生成氢氧化铝胶体,可用作水的净化剂 | |
| C. | Na2CO3溶液具有碱性,可用热的浓Na2CO3溶液洗涤试管内壁的油污 | |
| D. | Mg(OH)2受热分解生成H2O和MgO且△H>0,可用Mg(OH)2作阻燃剂 |
17.下列过程属于人工固氮的是( )
| A. | 分离液态空气制氮气 | |
| B. | 闪电将空气中的N2转化成NO | |
| C. | 工业上合成氮 | |
| D. | 豆科植物将空气中的N2转化为化合态氮 |
14.一种甲醇、氧气和强碱溶液做电解质的新型手机电池,可连续使用一个月.该电池反应为:2CH3OH+3O2+4OH-$?_{充电}^{放电}$2CO32-+6H2O,则有关说法正确的是( )
| A. | 充电时阴极发生氧化反应 | |
| B. | 放电时负极的电极反应为CH3OH+8OH--6e-═CO32-+6H2O | |
| C. | 通入0.25mol氧气并完全反应后,有1mol电子转移 | |
| D. | 放电时阴离子向正极移动 |
1.试推测该有机物CH3CH(OH)CH=CHCOOH不可能具有的性质是( )
| A. | 能与碳酸钠反应产生气体 | B. | 能被酸性高锰酸钾氧化 | ||
| C. | 能发生酯化反应 | D. | 能发生水解反应 |
11.下列说法错误的是( )
| A. | 乙醇的水溶液可使蛋白质发生性质改变 | |
| B. | 纤维素在一定条件下水解生成葡萄糖 | |
| C. | 在一定条件下油脂水解可生成甘油 | |
| D. | 煤的干馏、石油的分馏都属于化学变化 |
18.苹果酸的结构简式为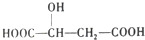 ,下列说法错误的是( )
,下列说法错误的是( )
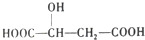 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 1mol苹果酸可与2 molNaOH发生中和反应 | |
| B. | -定条件下,苹果酸与乙酸或乙醇均能发生酯化反应 | |
| C. |  与苹果酸互为同分异构体 与苹果酸互为同分异构体 | |
| D. | 1mol苹果酸与足量金属Na反应生成1.5 molH 2 |
15.下列离子方程式表达正确的是( )
| A. | 向氯化铁溶液中滴加HI溶液:2Fe3++2HI═2Fe2++2H++I2 | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(0H)2恰好使反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4+AlO2-+2H2O | |
| C. | 1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积均匀混合2AlO2-+5H+═Al(OH)3+Al3++H2O | |
| D. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2═I2+2OH- |
16.下列实验的原理分析中,正确的是( )
| A. | 将SO2通入品红溶液或者溴水都能使它们褪色,均说明SO2具有漂白性 | |
| B. | 蘸有浓氨水和蘸有浓HNO3的玻璃棒靠近时有白烟产生,是因为氨气有还原性 | |
| C. | 某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,说明溶液中一定没有NH4+ | |
| D. | NH3•H2O的热不稳定性可以解释实验室中用加热氨水的办法制取氨气 |