题目内容
【题目】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质, C、F是无色无味的气体,H是白色沉淀,.
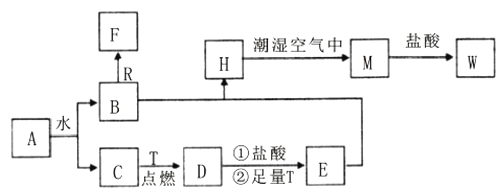
(1)H在潮湿空气中变成M的实验现象是______________,化学方程式为________。
(2)A和水反应生成B和C的离子方程式为___________________________,由此反应可知A有作为_________的用途。
(3)步骤①的离子方程式_________________________,步骤②后的离子方程式___________________请写出检验W溶液中主要阳离子所需要的试剂:_____。
(4)B和R在溶液中反应生成F的离子方程式为_____________________
【答案】白色沉淀迅速变为灰绿色,最终变为红褐色 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3 2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑ 供氧剂 Fe3O4+8H+ = Fe2++2Fe3++ 4H2O Fe + 2Fe3+ =3Fe2+ KSCN 2Al+2OH-+2H2O=2AlO2-+3H2↑
【解析】
依据转化关系和反应条件,A为淡黄色固体且能与水反应,所以A为Na2O2,则C为O2,B为NaOH;R是地壳中含量最多的金属,则R为Al,Al可以与NaOH反应产生无色无味的气体F,则F为H2;T为生活中使用最广泛常的金属单质,则T为Fe;Fe在氧气中燃烧生成Fe3O4,则D为Fe3O4;D与盐酸反应再与铁反应生成E为FeCl2,FeCl2结合NaOH反应生成白色沉淀Fe(OH)2,则H为Fe(OH)2,Fe(OH)2与潮湿的空气反应生成Fe(OH)3,则M为Fe(OH)3,M与盐酸反应会生成FeCl3,则W为FeCl3,再根据各物质的性质分析作答。
根据上述分析可知:
(1)H在潮湿空气中变成M的实质是Fe(OH)2转化为Fe(OH)3的过程,其实验现象为白色沉淀迅速变为灰绿色,最终变为红褐色,发生的化学方程式为:4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3,
故答案为:白色沉淀迅速变为灰绿色,最终变为红褐色;4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3;
(2)A为Na2O2,与水反应的离子方程式为:2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑;Na2O2可与水或二氧化碳制备氧气,故可作为供氧剂,
故答案为:2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑;供氧剂;
(3)D为Fe3O4,D与盐酸反应会生成氯化铁与氯化亚铁和水,其离子方程式为:Fe3O4+8H+ = Fe2++2Fe3++ 4H2O;再加入足量单质铁以后,溶液中的Fe3+会被还原为Fe2+,其离子方程式为:Fe + 2Fe3+ =3Fe2+;W为FeCl3,Fe3+可使KSCN溶液变红,则检验W溶液中主要阳离子所需要的试剂为KSCN溶液,
故答案为:Fe3O4+8H+ = Fe2++2Fe3++ 4H2O;Fe + 2Fe3+ =3Fe2+;KSCN;
(4)B为NaOH,R为Al,则两者在溶液中反应生成F(H2)的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】已知:CO(g) + H2O(g) ![]() H2(g) + CO2(g) 的平衡常数K随温度的变化如下表,下列说法正确的是( )
H2(g) + CO2(g) 的平衡常数K随温度的变化如下表,下列说法正确的是( )
温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
A. 该反应的正反应是吸热反应
B. 恒温时增大压强,正反应速率增大
C. 830℃时,反应达到平衡,一定是c(CO)=c(CO2)
D. 400℃时,生成CO2物质的量越多,平衡常数K越大
【题目】X、Y、Z、M、W、Q、R是7种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | W | Q | R |
原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
主要化合价 | +1 | +3 | +6,﹣2 | +7,﹣1 | +5,﹣3 | ﹣2 | +1 |
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是________________________________;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是_______(填离子符号)。
W和R按原子个数比1﹕4构成的阳离子所含的化学键是____________________。
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是_______(填化学
式),其电离方程式为_____________________________________。
(3)M与Z相比,非金属性较强的是_____________(填元素名称),请从原子结构的角度说明理由_________________________________________________________________。
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
![]() KMnO4+
KMnO4+![]() H2O2+
H2O2+![]() H2SO4 →
H2SO4 → ![]() K2SO4+
K2SO4+![]() MnSO4+
MnSO4+![]() O2↑+
O2↑+![]() H2O
H2O
请配平,当有0.5 mol H2O2参加此反应,电子转移的个数为______________________。