题目内容
2.铁不能与冷水、热水反应,但能与高温水蒸气反应,化学方程式: ,用单线桥法分析上述反应.
,用单线桥法分析上述反应.
分析 高温条件下,Fe和水蒸气发生氧化还原反应生成四氧化三铁和氢气,该反应中Fe元素化合价由0价变为+2价、+3价,H元素化合价由+1价变为0价,转移电子数为8,据此分析解答.
解答 解:高温条件下,Fe和水蒸气发生氧化还原反应生成四氧化三铁和氢气,该反应中Fe元素化合价由0价变为+2价、+3价,H元素化合价由+1价变为0价,转移电子数为8,其电子转移方向和数目为 ,
,
故答案为: .
.
点评 本题考查化学方程式的书写,为高频考点,明确反应物、生成物及反应条件即可解答,注意该反应中转移电子数的计算,知道四氧化三铁中Fe元素化合价,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列反应的离子方程式正确的是( )
| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铝片插入硝酸汞溶液中:Al+Hg2+=Al3++Hg | |
| C. | Ba(OH)2与稀H2SO4反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 盐酸除铁锈:O2-+2H+═H2O |
7.用1L 1mol•L-1NaOH溶液吸收0.8molCO2,所得溶液中n(Na2CO3)和n(NaHCO3)之比约为( )
| A. | 1:3 | B. | 3:1 | C. | 2:3 | D. | 3:2 |
2.对废锌渣(主要成分是ZnO、FeO、Fe2O3、CuO)进行适当处理可制得ZnSO4•7H2O,其流程如图.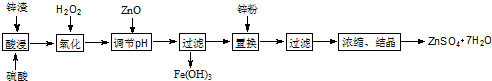
(1)酸浸时温度和时间对锌浸出率的影响如表.
 综合考虑,反应的最佳温度和时间是2h、90℃
综合考虑,反应的最佳温度和时间是2h、90℃
(2)氧化时也可改通空气,其原因是4Fe2++O2+4H+═4Fe3++2H2O.(用离子方程式表示)
(3)加入锌粉的目的是除去Cu2+.
(4)检验Fe3+是否除尽的方法是取第一次过滤后的滤液少许于试管中,加KSCN溶液,若溶液无血红色出现,则Fe3+已除尽.
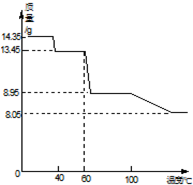
(5)取14.35gZnSO4•7H2O加热分解,加热过程中,固体质量随温度的变化如图所示.写出从60℃到80℃时发生的反应ZnSO4•6H2O$\frac{\underline{\;△\;}}{\;}$ZnSO4•H2O+5H2O.(用化学方程式表示)

(1)酸浸时温度和时间对锌浸出率的影响如表.
| 酸浸时间/h | 酸浸温度/℃ | 锌浸出率/% |
| 2 | 80 | 87 |
| 2 | 90 | 95 |
| 2 | 110 | 85.3 |
| 3 | 95 | 94.5 |
| 2.5 | 95 | 94 |
 综合考虑,反应的最佳温度和时间是2h、90℃
综合考虑,反应的最佳温度和时间是2h、90℃(2)氧化时也可改通空气,其原因是4Fe2++O2+4H+═4Fe3++2H2O.(用离子方程式表示)
(3)加入锌粉的目的是除去Cu2+.
(4)检验Fe3+是否除尽的方法是取第一次过滤后的滤液少许于试管中,加KSCN溶液,若溶液无血红色出现,则Fe3+已除尽.
(5)取14.35gZnSO4•7H2O加热分解,加热过程中,固体质量随温度的变化如图所示.写出从60℃到80℃时发生的反应ZnSO4•6H2O$\frac{\underline{\;△\;}}{\;}$ZnSO4•H2O+5H2O.(用化学方程式表示)
20.将500mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol NaOH的烧碱溶液,恰好完全反应;另取一份加入含b mol HCl的盐酸,恰好完全反应.则该混合溶液中c(Na+)(单位:mol•L-1)为( )
| A. | $\frac{2b-a}{20}$ | B. | 2b-a | C. | 5b-$\frac{5a}{2}$ | D. | 10b-5a |
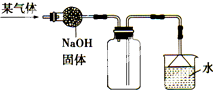 如图是收集某气体的装置.由实验装置推测该气体的有关性质可能正确的是( )
如图是收集某气体的装置.由实验装置推测该气体的有关性质可能正确的是( )