题目内容
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
A 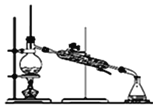 B
B 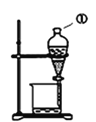 C
C 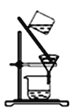 D
D 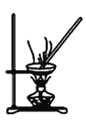
(1)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的字母,下同)。
(2)A装置中插有温度计的玻璃仪器名称为______。
(3)从碘水中分离出I2选择装置______,分离方法的名称为____、______。
(4)装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是_____。
(5)在实验室中取少量海水,进行如下流程的实验:
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
粗盐中含Ca2+、Mg2+、Fe3+、SO42—等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④用适量盐酸调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是____________(填选项字母)。
a.⑤③①⑥②④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(6)粗盐的提纯实验中每步所加试剂均需过量,如何判断除杂过程中所加BaCl2溶液是否过量?_______。
【答案】D 蒸馏烧瓶 B 萃取 分液 应先将分液漏斗上的活塞拿下后再打开旋塞放出液体或者使分液漏斗活塞上的凹槽对准分液漏斗口上的小孔后再打开旋塞放出液体 d 取加入过量的BaCl2溶液后的上层清液少许于试管中,滴入BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
【解析】
由图可知,A为蒸馏,B为萃取分液,C为过滤,D为蒸发。
(1)蒸发可以实现易溶于水的固体和水的分离,从氯化钾溶液中得到氯化钾固体可用蒸发,故答案为:D;
(2)A装置为蒸馏,插有温度计的玻璃仪器名称为蒸馏烧瓶,故答案为:蒸馏烧瓶;
(3)碘微溶于水,碘易溶于苯、四氯化碳等有机溶剂,且苯、四氯化碳与水互不相溶,可用萃取分液法分离,从碘水中分离出I2选择装置为B,故答案为:B;萃取;分液;
(4)装置B在分液时为使液体顺利滴下,应使分液漏斗内压强与外界气压相等,具体操作为应先将分液漏斗上的活塞拿下后再打开旋塞放出液体或者使分液漏斗活塞上的凹槽对准分液漏斗口上的小孔后再打开旋塞放出液体,故答案为:应先将分液漏斗上的活塞拿下后再打开旋塞放出液体或者使分液漏斗活塞上的凹槽对准分液漏斗口上的小孔后再打开旋塞放出液体;
(5)粗盐的提纯实验中每步所加试剂均需过量,除去粗盐中的可溶性杂质Mg2+、Ca2+、Fe3+、SO42-时,先加水溶解,所以加入过量NaOH溶液去除镁离子和铁离子;加入过量BaCl2溶液除去硫酸根离子;加入过量Na2CO3溶液除去钙离子和加入过量氯化钡溶液引入的钡离子,碳酸钠必须加在氯化钡溶液之后,氢氧化钠溶液和氯化钡溶液可以颠倒加入的顺序,然后过滤,最后用适量盐酸调节溶液的pH等于7,蒸发即可,所以其顺序是⑤③②①⑥④⑦或⑤②③①⑥④⑦,故答案为:d;
(6)判断加入BaCl2已过量的方法是继续加入氯化钡溶液,即在加入过量的BaCl2溶液后的上层清液中,再滴入BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量,故答案为:取加入过量的BaCl2溶液后的上层清液少许于试管中,滴入BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.2kJ/mol
2NH3(g) ΔH=-92.2kJ/mol
(1)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2 | H2 | NH3 | |
投料Ⅰ | 1.0 mol/L | 3.0 mol /L | 0 |
投料Ⅱ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数表达式为_____________。
②按投料Ⅱ进行反应,起始时反应进行的方向为________(填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数________(填“变大”、“变小”或“不变”)。
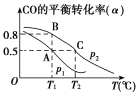
(2)L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。
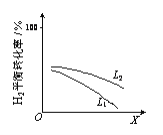
ⅰ X代表的物理量是______。
ⅱ 判断L1、L2的大小关系,并简述理由:______。
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:
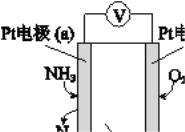
① 电极b上发生的是______反应(填“氧化”或“还原”)
② 写出电极a的电极反应式:_________。